NEJM综述:多发性骨髓瘤研究进展
2011-04-05 MedSci原创 MedSci原创
多发性骨髓瘤是一种肿瘤浆细胞病,其特征是骨髓微环境中恶性浆细胞的克隆性增生,血液或尿中存在单克隆蛋白,以及伴随的器官功能障碍1。它大约占肿瘤性疾病的1%以及血液系统癌症的13%。在西方国家,经年龄校正的年发病率为5.6例/10万人2。诊断时年龄的中位数大约为70岁,37%的病人年龄<65岁,26%的病人年龄在65~74岁之间,以及37%的病人年龄≥75岁2,3。近年来,自体干细胞移植以及药物[
多发性骨髓瘤是一种肿瘤浆细胞病,其特征是骨髓微环境中恶性浆细胞的克隆性增生,血液或尿中存在单克隆蛋白,以及伴随的器官功能障碍1。它大约占肿瘤性疾病的1%以及血液系统癌症的13%。在西方国家,经年龄校正的年发病率为5.6例/10万人2。诊断时年龄的中位数大约为70岁,37%的病人年龄<65岁,26%的病人年龄在65~74岁之间,以及37%的病人年龄≥75岁2,3。近年来,自体干细胞移植以及药物[例如沙利度胺、来那度胺(lenalidomide)和硼替佐米)]的可用性已改变了骨髓瘤的管理并延长了(病人的)总生存(时间)3-5。在60岁以下就诊的病人中,10年生存(率)约为30%4。
多发性骨髓瘤的生物学
骨髓瘤可由无症状的单克隆浆细胞恶变前增生引起,这些单克隆浆细胞来源于生发中心后B细胞。多步骤遗传和微环境改变可导致这些细胞转化为恶性肿瘤。骨髓瘤最常被认为可从1种未确定临床意义的单克隆丙种球蛋白病(通常被称为MGUS)演变而来,后者可进展为郁积型(无症状)骨髓瘤(smoldering myeloma),并最终进展为有症状的骨髓瘤(图1)6。发生于肿瘤浆细胞中的数种遗传异常在骨髓瘤的发病机制中起重要作用 7。

主要的早期染色体易位发生在染色体14(q32.33)上的免疫球蛋白(Ig)转换区,该区最常与染色体4p16.3上的MAF[t(14;16)(q32.33;23)]和MMSET并列。该过程可导致两个毗邻基因的失调,所有病例中的MMSET以及30%病例中的FGFR3(存在这种失调)6,8。参与疾病进展的次要迟发性易位和基因突变包括MYC的复杂核型异常,NRAS和KRAS的激活,FGFR3和TP53突变,以及周期蛋白依赖激酶抑制基因CDKN2A和CDKN2C的失活6,8。其他的基因异常包括表观遗传调节异常,例如微小RNA表达和基因甲基化修饰的改变9。根据基因异常,基因表达谱允许将多发性骨髓瘤分为不同的亚类10。(本文中所有基因的全名均在补充附录的词汇表中提供,其与本文全文均可在NEJM.org获取)
基因异常可改变骨髓瘤细胞上黏附分子的表达以及对微环境中生长刺激的反应(图2)。骨髓瘤细胞和骨髓细胞或细胞外基质蛋白之间的相互作用[通过细胞表面受体介导,例如整联蛋白、钙黏着蛋白、选凝素(selectin)和细胞黏附分子],可使肿瘤的生长、生存(期)、迁移和耐药性增加。骨髓瘤细胞黏附于造血细胞和基质细胞可诱导细胞因子和生长因子的分泌,包括白介素-6、血管内皮生长因子(VEGF)、胰岛素样生长因子1、肿瘤坏死因子超家族成员、转化生长因子β1和白介素-10。这些细胞因子和生长因子由骨髓微环境中的细胞(包括骨髓瘤细胞)产生和分泌,并且受自分泌和旁分泌环的调节11。
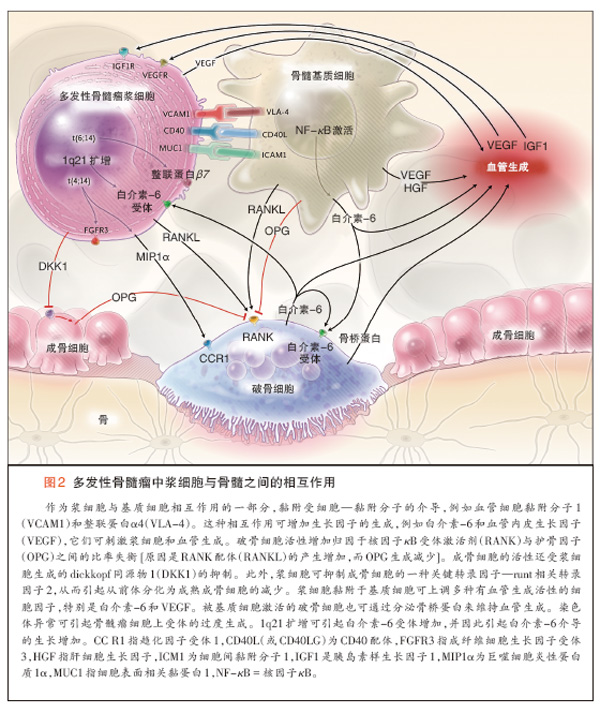
骨髓瘤细胞黏附于细胞外基质蛋白(例如胶原、纤连蛋白、层粘连蛋白和玻连蛋白)可触发细胞周期调节蛋白和抗细胞凋亡蛋白的上调12。骨病变由成骨细胞和破骨细胞的功能失衡引起。抑制Wnt途径可抑制成骨细胞,而扩增RANK途径以及巨噬细胞炎症蛋白1α(MIP1α)的作用可激活破骨细胞13。诱导促血管生成分子(例如VEGF)可增强骨髓微血管的密度,并可以解释骨髓瘤肿瘤血管异常结构的原因12。
蛋白酶体抑制剂和免疫调节药的抗骨髓瘤活性可由多个信号转导通路的破坏产生,这些通路支持骨髓瘤细胞的生长、增殖和和生存。蛋白酶体抑制可刺激多个细胞凋亡途径,包括诱导内质网应激反应,以及通过抑制核因子κB(NF-κB)信号下调血管生成因子、细胞因子信号和微环境中的细胞黏附14。免疫调节药可刺激细胞凋亡并抑制血管生成、黏附和细胞因子的回路。它们还可通过刺激宿主的T细胞和自然杀伤细胞,来对骨髓瘤细胞产生一种增强的免疫反应15。
临床表现、诊断和分期
骨髓瘤的诊断依据是,血清或尿中至少存在10%的克隆骨髓浆细胞和单克隆蛋白。在有真正的非分泌性骨髓瘤的病人中,诊断的依据是存在30%的单克隆骨髓浆细胞或经活检证实的浆细胞瘤16。骨髓瘤被分类为无症状或有症状,这取决于是否存在骨髓瘤相关器官或组织的功能障碍,包括高钙血症、肾功能不全、贫血和骨病(表1)16-18。贫血(诊断时存在于大约73%的病人中)通常与骨髓瘤的骨髓浸润或肾功能不全有关19。骨性病变可发生在几乎80%有新诊断疾病的病人中。在一项研究中,58%的病人报告了骨痛20。肾损伤发生于20%~40%有新诊断疾病的病人中20,21主要原因是蛋白质负荷过多、脱水、高钙血症和使用肾毒性药物导致的直接肾小管损伤22。感染的危险因活动性疾病而增加,但因为对治疗有疗效反应而降低23。高钙血症不常见20。

为了诊断骨髓瘤,推荐进行的试验包括采集详细的医疗史和体检,常规的实验室检测(全血细胞计数、化学分析、血清和尿蛋白免疫固定电泳,以及单克隆蛋白的定量测定),以及骨髓检查[环钻活检加抽吸物细胞遗传学分析或荧光原位杂交(FISH)检测] 18,24。脊柱、颅骨、胸部、骨盆、肱骨和股骨的常规 X线片检查仍是辨别骨髓瘤相关骨病变的标准。在常规X线片检查结果正常的病人中,以及在所有X线片提示存在孤立性骨浆细胞瘤的病人中,有人推荐用磁共振成像(MRI)评估症状。计算机体层摄影(CT)和MRI是评估怀疑脊髓压迫的首选检查步骤,应被紧急实施18,25。
其他检查包括按照国际分期系统进行的疾病分期,该系统根据血清β2-微球蛋白和白蛋白水平界定了3个危险组26。与有正常核型者的转归相比,标准细胞遗传学分析时检出的任何染色体异常,均与(病人)转归差相关24。FISH检测时检出的免疫球蛋白重链区中的特定易位[例如t(4;14),17p13缺失和染色体1异常]与预后差相关7。最近,基因表达谱和基因拷贝数改变已显示出一种有前景的预测作用,这种作用需要在较大型的研究中得到验证24。高危疾病和预后差用是否存在以下每个范畴中的1种来定义:低二倍性,t(4;14)或17p13缺失;高水平的血清β2-微球蛋白或乳酸脱氢酶;以及国际分期系统Ⅲ期。标准危险疾病用是否存在以下指标来定义:超二倍性或t(11;14),正常水平的血清β2-微球蛋白或乳酸脱氢酶,以及国际分期系统Ⅰ期 24,26,27。

治疗
策略
对有症状的(活动性)疾病应立即治疗,而无症状(郁积型)骨髓瘤仅需临床观察,因为用常规化疗进行的早期治疗已显示无益处1,28,29。目前研究性试验正在评估免疫调节药延缓从无症状发展至有症状骨髓瘤的能力。治疗策略主要与年龄有关30。对于年龄<65岁并且没有重大心、肺、肾或肝功能障碍的病人,目前的数据支持开始用沙利度胺、lenalidomide或硼替佐米的诱导治疗加造血干细胞移植31。对于年纪较大的病人或有共存病的病人,应考虑采用降低预处理强度方案的自体干细胞移植32,33。在年龄>65岁的病人中,医师应给予常规治疗联合沙利度胺、lenalidomide或硼替佐米33。在年龄>75岁的病人中,或者在有共存病的较年轻病人中,应考虑(治疗)强度较小的方法,这种方法可限制毒性效应或防止会降低预期疗效的治疗中断。应根据生物学年龄(有可能不同于实足年龄),以及存在共存病决定治疗选择和药物剂量。
治疗策略应包括使用与完全缓解率高相关的诱导方案,然后进行维持治疗。该方法可将最大程度的肿瘤缩小与连续治疗相结合,这对延缓肿瘤再生是必不可少的。应答的水平(特别是获得完全缓解)与改善长期转归相关。一次完全缓解的定义是:常规检测时已消除了可检出疾病16-18。已有人探索了较严格的标准(例如血清游离免疫球蛋白轻链的定量测定34,用多参数流式细胞计数仪对骨髓骨髓瘤细胞进行定量测定,以及聚合酶链反应测定时辨别残余肿瘤细胞),以定义最小残余疾病,后者是(病人)生存的最重要独立预后因素之一35,36。自体移植后出现一次完全缓解的较年轻病人,具有延长的无进展生存期和总生存期 37,38。一项回顾性分析包括了1175例病人,他们接受了美法仑和泼尼松加硼替佐米或沙利度胺的联合治疗,结果显示,在随访中位时间29个月以后,与没有发生过完全缓解的病人相比,出现过一次完全缓解病人的死亡危险减少了75%39。用2~4个周期的联合治疗进行巩固,并用单药进行维持治疗直至疾病进展,有可能改善(病人的)转归。自体移植后用基于硼替佐米或基于lenalidomide的方案进行巩固治疗,可显著提高完全缓解率32,36。用沙利度胺(尽管受到发生外周神经病的限制)40-44,或者用最近可获得的药物lenalidomide进行维持治疗,改善了较年轻和老年病人中的无进展生存情况45-47。
最近的治疗趋势支持根据一例具体病人的危险因素对治疗进行修改。虽然这种危险适应性策略尚未获得前瞻性的证实,但某些研究者建议对高危疾病使用含硼替佐米的治疗方案,以及对标准危险疾病使用含lenalidomide或沙利度胺的治疗方案27,48,49。这些推荐意见是基于以下证据:有 t(4;14)并接受lenalidomide和地塞米松联合治疗病人的总生存期比没有t(4;14)的病人短50。相反,硼替佐米诱导(治疗)改善了有 t(4;14)病人的生存期,但未改善有17p13缺失者的生存期51。
在符合移植条件病人中的诱导治疗
表2和补充附录中的表1提供了诱导治疗的详细描述52-76。治疗方法的概览见图3(见下期)。将沙利度胺、lenalidomide或硼替佐米引入诱导方案已使完全缓解率增高。有人推荐进行3~6个周期的诱导治疗31。在自体干细胞移植前,用地塞米松加沙利度胺52、硼替佐米53或 lenalidomide54进行的联合治疗,已被广泛用作一种诱导治疗方案,并且已使接近完全缓解率分别达到8%、15%和16%。最近,有人已引进了硼替佐米—地塞米松加多柔比星55、环磷酰胺56、沙利度胺57或lenalidomide56的三药联合疗法,接近完全缓解率分别为7%、39%、 32%和57%。在一项随机研究中,就应答率和无病生存而言,硼替佐米、沙利度胺和地塞米松的联合疗法优于沙利度胺加地塞米松的疗法57。在这类治疗方案中,地塞米松的剂量有可能不同,并且尽管因为使用了一种剂量强度较强的方案使应答的程度和速度增加,但由于毒性效应的危险显著较高而使生存情况未获改善 54。大剂量地塞米松(480 mg/月)的使用应限于有危及生命的高钙血症、脊髓压迫、初期肾功能衰竭或广泛疼痛的病人,否则应考虑较小剂量(地塞米松)(160 mg/月)31,54。

所谓的总治疗方案,即将所有可获得的药物用作诱导治疗,然后进行两个周期的大剂量治疗(美法仑,每剂为200 mg/m2)和自体外周血干细胞的再输注(串连移植),已使4年无事件生存率高达78%59,但没有随机研究支持这些结果。串连移植的益处是否超过了单次移植还不清楚60,61。对于大多数病人单次移植似乎是一种较适合的选择,因为高应答率可通过使用包括沙利度胺、lenalidomide或硼替佐米的诱导治疗方案获得,而且有可能通过移植后巩固治疗和维持治疗获得进一步提高31。(先进行)中间剂量的美法仑(100~140 mg/m2体表面积)治疗,然后实施自体(干细胞)移植,可被用于年龄65~70岁或有共存病的较年轻病人32,33。
无论在诊断时还是在复发时实施移植,(病人的)总生存情况均相似,尽管早期移植可显著延长无进展生存期,以及延长无症状、无治疗和无治疗相关毒效应的时间62。一项前瞻性临床试验正在评估,用含沙利度胺、lenalidomide或硼替佐米的联合疗法进行诱导治疗以后,延迟移植(对病人)的影响63。
考虑到死亡和并发症的发生危险高,在临床试验以外应很少进行同种异体移植。然而,在经选择的病人中,它有可能实现长期的疾病控制。比较同种异体移植物与自体移植物的试验已产生了相互矛盾的结果。在高危病人中,未发现转归有显著差异64。在162例有新诊断疾病的病人中,与接受两次自体移植的病人(当没有同胞时)相比,正在接受自体—同种异体移植(串连移植,即先进行自体移植,然后在可以获得时,用来自一名合格的HLA完全一致同胞的移植物进行第二次移植)病人中报告的无事件生存(率)和总生存(率)增加65。
在不符合移植条件病人中的诱导治疗
一项荟萃分析涉及了包括1685例病人的多项研究,这些病人被选入6项比较美法仑加泼尼松(有或没有沙利度胺)的随机研究66-71,结果显示,增加沙利度胺使无进展生存期中位数延长了5.4个月,并使总生存期延长了6.6个月72。在一项大型、随机研究中,与仅使用美法仑和泼尼松相比,美法仑、泼尼松和硼替佐米的联合治疗使完全缓解率显著增高,并显著延长了至疾病进展的时间和总生存期73,74。美法仑和泼尼松加沙利度胺或硼替佐米的联合疗法,目前被认为是不符合移植条件病人的治疗标准。在包含糖皮质激素加沙利度胺或硼替佐米的联合治疗研究中,以及在环磷酰胺替代美法仑以减少血液学毒效应的研究中,应答率没有改变,但没有报告有关转归的数据43,56。一项随机研究显示,先用美法仑、泼尼松和lenalidomide联合治疗,然后用 lenalidomide维持治疗,优于仅用美法仑和泼尼松治疗。三药联合治疗的完全缓解率较高,而且用lenalidomide维持疗法延长了无进展生存期,但没有发现有生存差异。在年龄为65~75岁的病人中,与仅用美法仑和泼尼松的疗法相比,美法仑、泼尼松和lenalidomide的联合治疗(无 lenalidomide维持治疗)改善了无进展生存期,尽管在年龄>75岁的病人中未见差异47。
另一种联合治疗lenalidomide加地塞米松,与单纯使用大剂量地塞米松相比,增加了完全缓解率并延长了无进展生存期75。在一项比较 lenalidomide加小剂量或大剂量地塞米松的随机研究中,使用小剂量地塞米松改善了(病人的)生存情况,并减少了严重不良事件的发生率54。
因此,lenalidomide加小剂量地塞米松是以前治疗方案的一种备选方案。该疗法正在进行中的随机研究,与美法仑、泼尼松和沙利度胺联合治疗相比,应提供有关这些疗法的相对有效性和安全性特征。一种强度更大的治疗方法,先进行硼替佐米、美法仑、泼尼松和沙利度胺的4药联合治疗,然后用硼替佐米和沙利度胺进行维持治疗,已在老年病人中取得了空前的成功,3年无进展生存率达56%。为了进一步优化治疗,硼替佐米的剂量安排从每周输注2次减少到每周输注1次。硼替佐米每周输注1次的安排未能对无进展生存产生显著影响,但极大地降低了外周神经病的发生危险76,77。
巩固和维持治疗
虽然没有具体的指南,但巩固治疗(在诱导治疗后使用2~4个周期的联合治疗)和维持治疗(用单药进行连续治疗直至疾病进展)已被广泛接受。已有人报告,在自体移植后用4个疗程的联合治疗(硼替佐米、沙利度胺和地塞米松)进行巩固治疗,可使完全缓解率从15%增至49%36。数项随机研究已对自体移植或常规治疗后沙利度胺维持治疗的作用进行了探索。虽然生存益处并不总是显而易见,但在无进展生存率方面有改善。然而,长期沙利度胺暴露后的外周神经病发生危险,可限制其常规使用40-44。Lenalidomide有可能提供相同的益处而毒效应较少,而且极少的第二种癌病例已被报告。在包含曾接受自体移植病人的两项独立的随机研究中,与无维持治疗相比,lenalidomide维持治疗使(疾病)进展危险降低了54%和58%45,46。在用美法仑、泼尼松和lenalidomide联合治疗的老年病人中,与对照受试者中的危险相比,lenalidomide维持治疗使(疾病)进展危险减少了75%47。这一益处在所有类别的病人中都显而易见,并且独立于诱导治疗后获得的应答质量。虽然在维持治疗方案中,硼替佐米加一种免疫调节药的作用仍未得到阐明,但来自两项独立试验的结果均支持在老年病人中采用这种类型的治疗方法76,77。目前,lenalidomide似乎是维持治疗最合适的选择,而硼替佐米正在随机研究中得到评估55,57。迄今为止,还没有数据对维持治疗后难治性复发的潜在危险进行评估。
复发时的治疗
在治疗有复发性或难治性骨髓瘤的病人时,对以前治疗的应答质量和持续时间是最重要的预后因素。对以前的治疗产生一次完全缓解有可能需要对后续的复发进行重复治疗。有新诊断疾病并在2年复治后有过一次复发的病人,或者有复发性或难治性骨髓瘤并在缓解1年后其疾病复发的病人,有可能接受相同疗法的再次治疗。相反,在较短时间后有复发疾病的病人,应接受一种不同的疗法78。地塞米松和硼替佐米79,80或lenalidomide81,82的联合疗法是有复发性或难治性骨髓瘤病人的首选治疗。回顾性分析表明,与以后给予上述药物相比,首次复发时给予与(病人)转归优越相关79,83。自体移植术是诊断时未接受移植的病人,以及接受移植术并且其缓解的持续时间延长病人的一种选择84。
一项随机研究显示,使用硼替佐米和多柔比星脂质体(liposomal doxorubicin)的疗法优于单纯使用硼替佐米85。那项研究显示,包括硼替佐米和化疗的联合疗法,在体内有加性效应或协同效应。硼替佐米或lenalidomide加地塞米松的有效性似乎通过增加第三种药(例如环磷酰胺、美法仑或多柔比星)而有所提高,提示在公认的补救方案已被用尽或该病对治疗产生耐药时,这类联合疗法或许可被更多地用于临床实践33,86。即使在该病对沙利度胺、lenalidomide或硼替佐米耐药时,lenalidomide、 硼替佐米和地塞米松的联合治疗也可获得应答。沙利度胺加地塞米松是一种有效的补救治疗,不会诱发细胞减少,并且在该病的晚期阶段,或者当血液系统毒效应是一种担心时,在虚弱的病人中,似乎是一种有价值的选择78。
支持治疗
尽管肿瘤对治疗有反应,但当血红蛋白水平没有明显升高时,有人推荐在减轻贫血的治疗期间使用红细胞生成刺激剂87。骨痛需要全身性镇痛、局部措施以及化疗。疼痛的治疗应从使用非阿片类镇痛剂(例如对乙酰氨基酚)开始,应避免使用非类固醇类抗炎药,因为有肾损伤的潜在危险。当非阿片类镇痛剂无效时,应引进阿片类镇痛剂。初始治疗应包括(镇痛效果)弱的阿片类药(可待因),而(镇痛效果)较强的阿片类药(吗啡或羟考酮)留给(对治疗)有不充分疗效反应的病人88。
局部放疗对缓解骨痛有效,采用分割放射治疗可缓解91%~97%病人的疼痛89。病理性骨折通常需要外科稳定。经皮椎体成形术(是有椎体塌陷病人的一种选择)可减轻疼痛,但不能恢复椎骨的高度90。使用二膦酸盐可减少新的骨病变和病理性骨折。为了减少颌骨坏死的可能性,二膦酸盐疗法仅应连续使用2年,并且为了预防电解质失衡,应考虑同时使用钙和维生素D391。最近已有研究报告,在有新诊断疾病并接受唑来膦酸治疗的病人中有生存益处92。二膦酸盐治疗前一次全面的牙科检查,保持良好的口腔卫生,以及避免有创的口腔操作,均可减少颌骨坏死的危险93。
在有肾功能不全的病人中,可采用适当的液体治疗、尿液碱化、骨髓瘤的速效治疗,以及高钙血症、高尿酸血症和感染的治疗,来预防肾功能的进一步恶化22 以及肿瘤溶解综合征的发生。高钙血症需要用充分的液体、利尿药、糖皮质激素和二膦酸盐进行即刻治疗 94。在化疗最初的3个月期间或移植后(感染危险增加时)应考虑采用甲氧苄啶—磺胺甲唑预防法。阿昔洛韦预防法被推荐用于所有接受基于硼替佐米治疗的病人23。虽然对接种疫苗的益处仍有争议,但对可预防流感嗜血杆菌(感染)的疫苗接种应予以考虑。然而,针对肺炎链球菌和流感病毒的疫苗接种尚无效。静脉免疫球蛋白的使用留给有反复危及生命的感染或IgG水平极低的病人。
治疗相关不良事件的管理
当沙利度胺、lenalidomide或硼替佐米与常规化疗同时使用时,血液系统毒性效应相当常见,但当这些药仅与地塞米松一起使用时,血液系统毒性效应不太常见。粒细胞集落刺激因子可降低中性粒细胞减少的发生率。尽管使用了粒细胞集落刺激因子,但当中性粒细胞计数<500/mm3时应停止化疗,然后当中性粒细胞计数恢复到至少1000/mm3时,用适当减少的剂量重新开始(化疗)。同样,当血小板计数在25000/mm3以下时应中断治疗,并且当它升至50000/mm3时,在适当减少所涉及药物的剂量以后再重新开始治疗95。
在有新诊断疾病的病人中,当沙利度胺52,66-71或lenalidomide54,75与地塞米松或化疗联用时,静脉和动脉血栓形成的发生率升高。血栓预防需要在治疗的最初6个月进行。小剂量阿司匹林适用于血栓栓塞事件危险标准的病人;低分子量肝素或足量华法林是高危病人(即肥胖、不能活动、有一根中心静脉导管,或有血栓栓塞、心脏病、慢性肾病、糖尿病、感染或外科操作史的病人)的首选疗法。在治疗期间有血栓栓塞事件的病人应暂停治疗,并且应在(病情)改善或消退后重新开始96。使用硼替佐米不增加静脉血栓栓塞的危险97。
硼替佐米和沙利度胺可引起外周神经病66-71,73,76,79。Lenalidomide与严重的外周神经病极少相关47,54,81,82。沙利度胺和硼替佐米相关的神经病均为累积性和剂量依赖性的。医师应教会病人认识外周神经病。早期减少可疑药的剂量是治疗这种病症最有效的方法。轻度且无并发症的感觉异常仅需要减量。当发生严重的感觉异常或疼痛或感觉丧失而妨碍日常生活活动时,应停止治疗,然后当症状减轻时以较小的剂量重新开始治疗。通常需要剂量减半,并且每周2次的硼替佐米应减为每周1次(静脉)输注76,95,98。加巴喷丁和普瑞巴林可减轻神经系统症状。
在年龄>75岁的病人中,或者在有心、肺、肝或肾功能障碍的较年轻病人中,较小剂量的标准治疗方案有可能预防需要停止治疗的毒性效应(表3)。有人推荐经年龄校正的剂量减少:地塞米松应从每周40 mg减少至每周20 mg31,54,美法仑在第1~4天从0.25 mg/kg体重减至 0.18 mg/kg体重或0.13 mg/kg体重47,66-71,73,lenalidomide在第1~21天从25 mg减至15 mg95,沙利度胺从200 mg/d减至100 mg/d或50 mg/d66-71,以及硼替佐米(剂量为1.3 mg/m2)从每周静脉输注2次减至每周1次 76。

未来方向
正在进行的研究正将沙利度胺、lenalidomide或硼替佐米归入治疗方法中,以便通过以下方式进一步改善(病人的)转归:界定与最大程度的肿瘤缩小相关的联合疗法,评估可延缓肿瘤再生长的巩固治疗或维持治疗,以及确定哪种方案可在特定的病人亚组中提供益处,并有良好的副作用特征。研究者正在努力制定危险适应性策略,在这些策略中,治疗有可能以对遗传多态性或(基因)突变的了解为依据,这些遗传多态性或(基因)突变可调节疾病发病机制背后的分子途径99。新的蛋白酶体的抑制剂(carfizomib),免疫调节药(pomalidomide)、靶向治疗(NF-κB、MAPK和AKT抑制剂)、表观遗传制剂(组蛋白脱乙酰基酶抑制剂vorinostat和panobinostat),以及人源化单克隆抗体(elotuzumab和 siltuximab)目前正在临床试验中接受研究100。
结论
在西方国家,骨髓瘤的发生率有可能在不久的将来随着人口的老龄化而增加。最近沙利度胺、lenalidomide和硼替佐米的引进,已改变了治疗典范,并延长了有骨髓瘤病人的生存期。诊断时,在符合移植条件的病人中建议如下方案:先进行基于硼替佐米或lenalidomide的治疗,然后再进行自体移植。在不符合移植条件的病人中,建议使用美法仑和泼尼松加沙利度胺或硼替佐米的联合疗法。用沙利度胺或lenalidomide进行的维持治疗可改善(病人的)无进展生存,但需要较长期的随访来评估对总生存情况的影响。复发时,地塞米松加硼替佐米、lenalidomide或沙利度胺的联合治疗,或硼替佐米加多柔比星脂质体的联合疗法被广泛使用。在有费用限制的情况下,包含糖皮质激素、烷化剂或沙利度胺的联合治疗应是对治疗最低限度的要求。
(Multiple Myeloma. N Engl J Med 2011; 364:1046-60. March 17, 2011)
本文见:http://www.nejm.org/doi/full/10.1056/NEJMra1011442
拓展阅读:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#多发性#
62
#研究进展#
61