安慰剂效应太强,让一个创新药连续吃bie了
2023-12-23 MedSci原创 MedSci原创 发表于威斯康星
股价7年翻28倍,用仅百济1/10的员工数量,Efgartigimod 上市首年即实现 4 亿美元的销售额,研发出上市第二年就有望成为重磅炸弹的FIC的argenx公司,拥有爆品艾加莫德(Efgart
股价7年翻28倍,用仅百济1/10的员工数量,Efgartigimod 上市首年即实现 4 亿美元的销售额,研发出上市第二年就有望成为重磅炸弹的FIC的argenx公司,拥有爆品艾加莫德(Efgartigimod)。
作为全球首款获批上市的FcRn抑制剂,该药具备“A pipeline in a drug”潜质(与K药类似),面向10多个适应证连开临床试验,且推进速度很快,面向重症肌无力的已经上市,多项临床已步入中后期,核心技术优势在于使用美洲驼IgG1抗体,以及独有的anti-FcRn抗体结构,市场对该药给予了很大的预期。目前这款FcRn拮抗剂艾加莫德(卫伟迦®)也已经正式在国内上市,成为重症肌无力领域的关键药物。
然而,近期两大临床研究失败,一下子让argenx公司进入冰点,市值30天暴跌了百亿美金。而失败的原因,竟然都是安慰剂效应太强,强大药与实验药物媲美的地步! 这也说明,不要总说自己的药物疗效好,也要看看安慰剂,不要小瞧了!
7月因慢性炎性脱髓鞘性多发性神经根神经病(CIDP)的II期临床成功涨到300亿美金的市值。
然而,上个月底艾加莫德在原发性免疫性血小板减少症(ITP)的临床III期折戟,股价大跌近20%,接着又在12月20日宣布关于天疱疮的III期临床主要终点、次要终点皆未达到,再次暴跌25%。
安慰剂效应太强,艾加莫德“傻眼”
Efgartigimod 皮下注射剂(Efgartigimod PH20)则在 6 月 20 日刚获 FDA 批准上市。Efgartigimod 皮下注射剂使用 Halozyme 的 ENHANZE 药物递送技术,与重组人透明质酸酶 PH20(rHuPH20)共同配制。Efgartigimod 皮下注射剂的 BLA 的申请基于包括一项 III 期 ADAPT-SC 研究结果,该研究数据显示,在成年 gMG 患者中 Efgartigimod 皮下注射药效学作用非劣于 Efgartigimod(VYVGART)静脉输注。此外,该研究还表明,Efgartigimod 皮下注射具有和静脉注射一致的临床疗效改善。
在重症肌无力和CIDP两个适应证上接连成功后,让艾加莫德看到了更多的希望。然而艾加莫德近两个月却连续在另两项备受关注的适应证上折戟。有意思的是,都是皮下注射剂,问题都不是出在战略基本面上,然而都吃了临床开发不利的亏,安慰剂都太强。尤其是在本次针对天疱疮的试验中,当argenx研发团队发现用低于指南剂量的类固醇还能展现出强大的改善效果后,实在吓傻。
11 月 28 日,Argenx 宣布艾加莫德皮下注射剂治疗原发免疫性血小板减少症(ITP) III 期临床 ADVANCE-SC 研究未达到主要终点。此次试验失败的关键在于,能改善血小板水平的患者数量(13.7%)甚至比不上安慰剂组(16.2%),通俗来讲,安慰剂比起艾加莫德,反而有更好的凝血效果。
最近在被诊断和复发的中度至重度PV和落叶型天疱疮(PF)成人患者的研究也失败。
ADDRESSS是一项随机双盲、安慰剂对照的全球多中心III期临床,旨在评估艾加莫德皮下注射剂在治疗被诊断和复发的中度至重度PV和落叶型天疱疮(PF)成人患者的疗效,共222名PV (n=190)或PF (n=32)成年患者,以2:1的比例随机接受艾加莫德和安慰剂的治疗。
值得注意的是,在安慰剂择定上,由于天疱疮目前没有特效药,首选药物是糖皮质激素,于是argenx在临床开发上做了一个选择,无论是艾加莫德治疗组,还是安慰剂组,患者都是在使用皮质类固醇(糖皮质激素)的基础上使用,然而重点在于,注入的是皮质类固醇最小剂量(CRmin),argenx原本预计从使用低于CR指南剂量开始,可以为艾加莫德创造足够的发挥空间,展示出疗效。而设定的主要终点是在连续两个月使用CRmin基础上能达到完全临床缓解的PV患者比例。
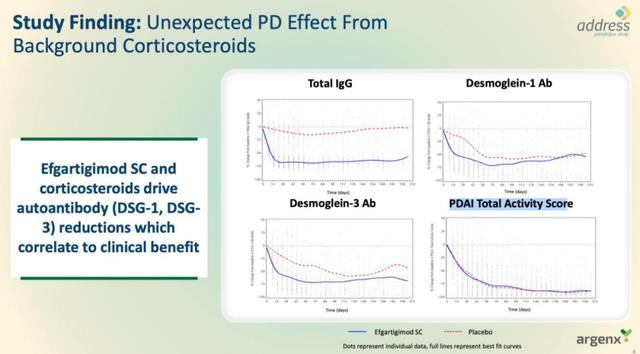
然而最终结果是,艾加莫德治疗组达成CRmin的PV患者比例为35.5%,安慰剂组为30.3% 。尽管艾加莫德依然降低了 IgG比例(75%),但真正的亮点却被安慰剂皮质类固醇夺走。既往文献中,类固醇使总IgG减少约10%,然而在此次试验中,使用的剂量是治疗指南中推荐剂量的1/3至1/2,但类固醇将抗DSG-1和DSG-3自身抗体减少了60%至70%,能有效改善临床结果。
这也提示,低剂量的类固醇进行皮下注射,依然展现出巨大的治疗效果! 在强大的作用背景下,艾加莫德的效应竟然有些被掩盖了。
接下来,argenx将停止对应ADDRESS研究的继续开发,优先考虑皮下注射剂在其进行中的严重自免适应证中的临床开发。
此外,基于PV和大疱性类天疱疮(BP)两种适应证之间相似的生物学原理和试验设计,其针对BP的II/III 期 BALLAD 研究正在紧急调整临床策略,接下来将根据其试验动态作出进一步权衡。但比起大疱性类天疱疮,寻常型天疱疮PV对应患者群体更大,PV是天疱疮中最常见的类型,尤在欧美、日本常见,但argenx已经放弃了对应市场。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#原发免疫性血小板减少症# #天疱疮# #安慰剂效应# #研究设计# #艾加莫德#
102