Advanced Science:中国科学院陈策实团队发现RNF126调控DNA损伤修复反应的新机制
2022-12-28 iNature iNature 发表于上海
三阴性乳腺癌(TNBC)具有较高的分子异质性和转移潜力,预后效果较差。
三阴性乳腺癌(TNBC)具有较高的分子异质性和转移潜力,预后效果较差。因针对TNBC的治疗方式有限,放射(IR)治疗仍是淋巴结或脑转移患者的常见选择。因此,迫切需要制定策略来增强TNBC肿瘤对低剂量IR的敏感性。
2022年12月23日,中国科学院,昆明医科大学及北京大学等多单位合作,陈策实、蒋德伟及智旭共同通讯在Advanced Science 在线发表题为“RNF126-Mediated MRE11 Ubiquitination Activates the DNA Damage Response and Confers Resistance of Triple-Negative Breast Cancer to Radiotherapy”的研究论文,该研究报道了E3泛素连接酶RNF 126对IR诱导的ATR-CHK1途径激活以增强DNA损伤修复(DDR)的重要作用。
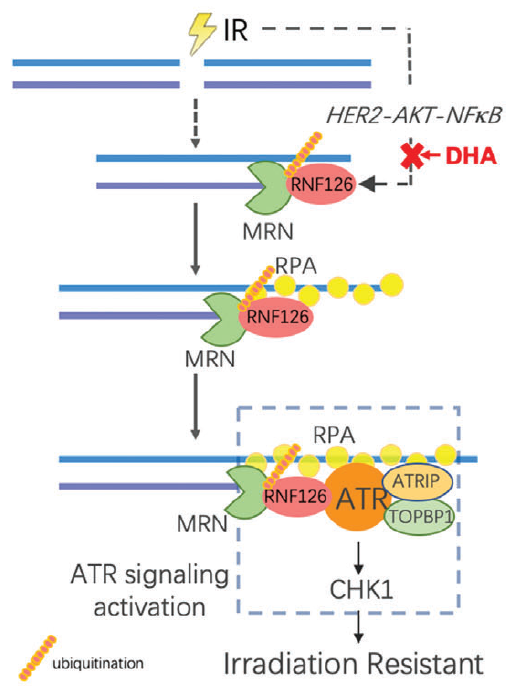
在机制上,RNF126与MRE11-RAD50-NBS1(MRN)复合物物理结合,并在K339和K480处使MRE11泛素化以增加其DNA核酸外切酶活性,随后的RPA结合和ATR磷酸化以同源重组修复的方式持续促进DDR。因此,RNF126的缺失导致TNBC细胞和小鼠的基因组不稳定性和放射敏感性增加。此外,研究发现IR激活HER2-AKT-NF-κB通路来诱导RNF126表达,双氢青蒿素靶向RNF126表达显著提高了脑部TNBC肿瘤对体内IR治疗的敏感性。总之,上述结果表明RNF126介导的MRE11泛素化是DDR的关键调节因子,为提高TNBC的放疗敏感性提供了希望靶点。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言