【衡道丨病例】一文详解!间变性甲状腺癌(Anaplastic Thyroid Carcinoma)如何诊断?
2024-02-09 衡道病理 衡道病理 发表于陕西省
今天就由上海交通大学医学院附属瑞金医院徐腾老师为大家分享间变性甲状腺癌的病理诊断要点。
患者病史
患者女性,92岁,半年前无明显诱因下自觉颏下肿块,近2月增大较快,伴疼痛,既往1997年行两次甲状腺癌切除术,2010年再次行甲状腺癌根治+胸大肌皮瓣修复术,后于2010年及2011年行2次同位素治疗,遂至我院就诊,查体见患者颏下肿块,质硬,活动度差,伴触痛,大小约直径5cm,无发热、咳嗽咳痰,胸闷气促等不适。一般状况良好。
影像检查
CT:
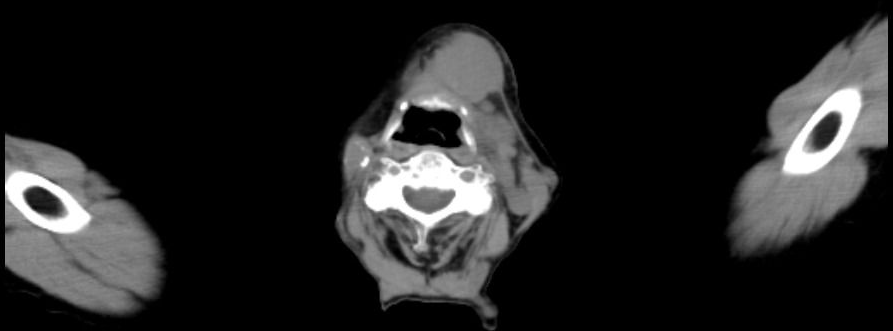
颏下偏左侧见大小约3.5cm×3.1cm软组织密度影,分界清,边缘光整,颏下及左侧颌下区淋巴结显示。
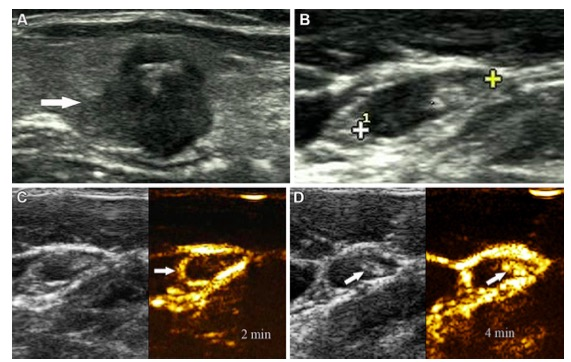
B超:
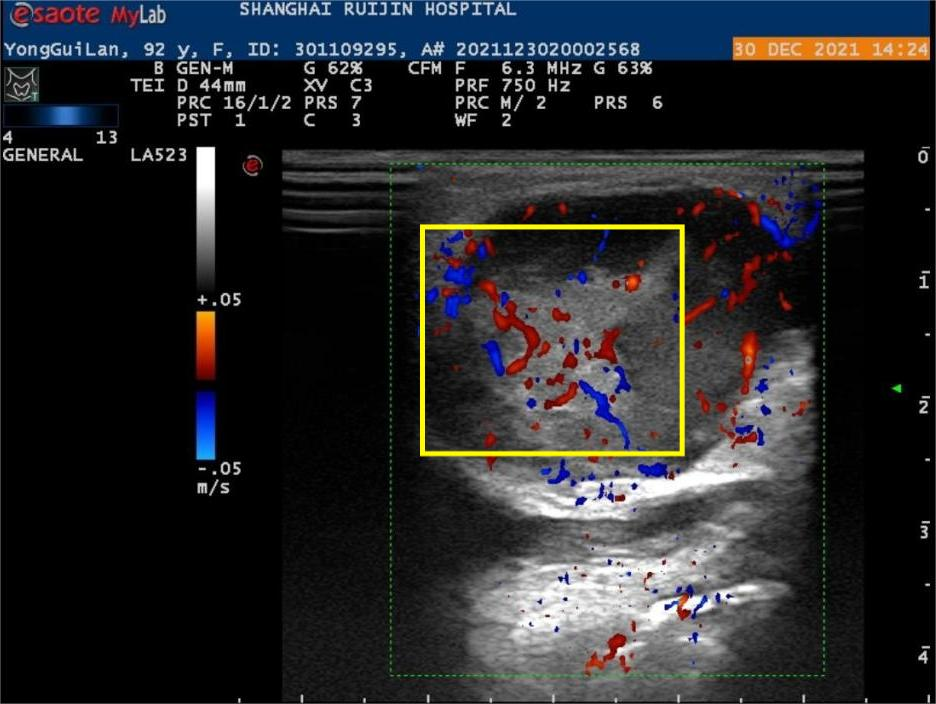
颏下区皮下软组织内可见一大小约 33.5×23.7×31.7mm团块,呈椭圆形,表面光整,境界清晰,内部呈低回声,分布不均,团块后方回声无明显改变,CFI示团块内部见较丰富血流信号。
大体形态
带皮肤组织一块,大小5.0×4.0×3.0cm,切开见一肿物,大小4.2×3.5×3.2cm,切面灰红灰白质中,界清,似有包膜。
镜下形态
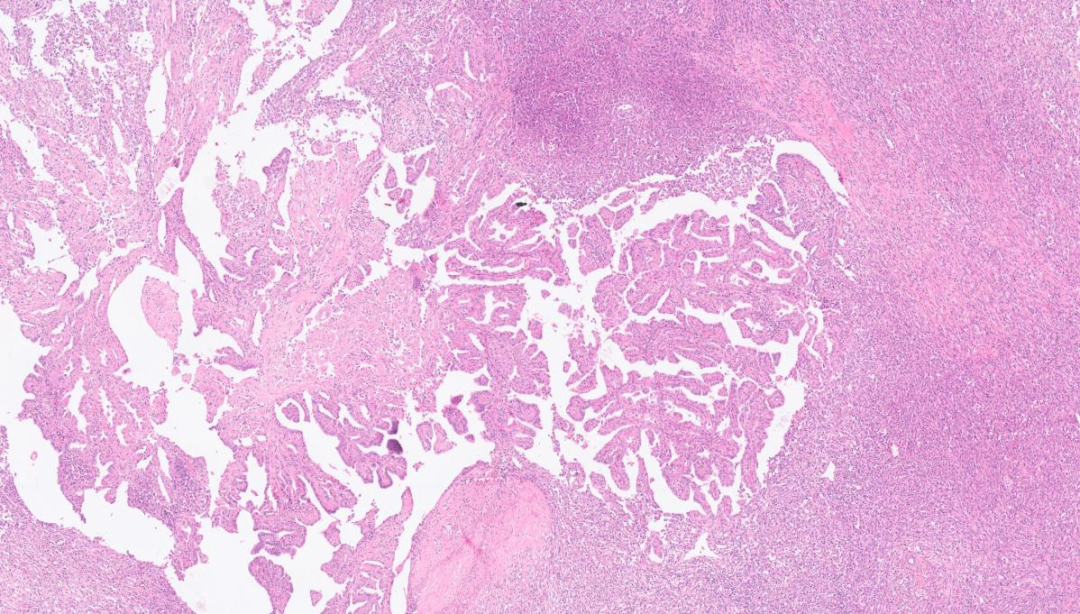
乳头区+实性区
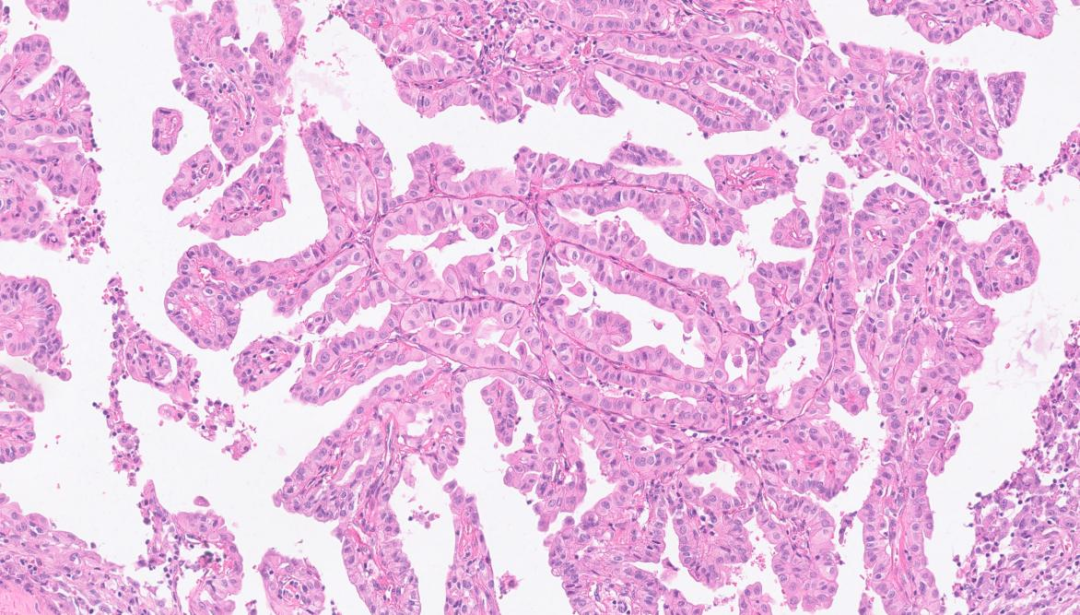
部分肿瘤细胞形成乳头状结构
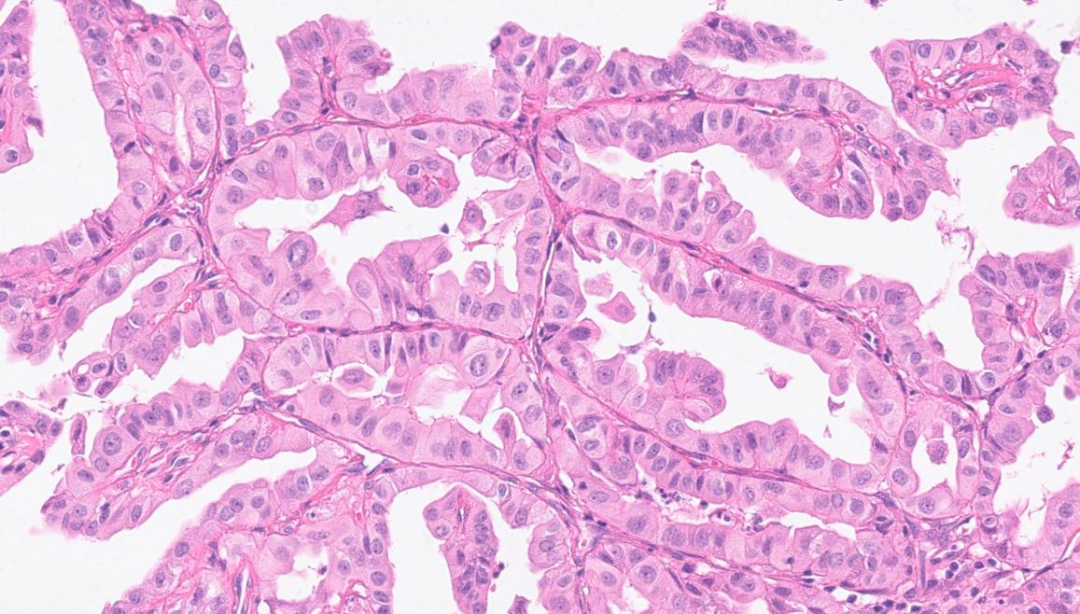
磨玻璃样细胞核,细胞长宽比>3:1
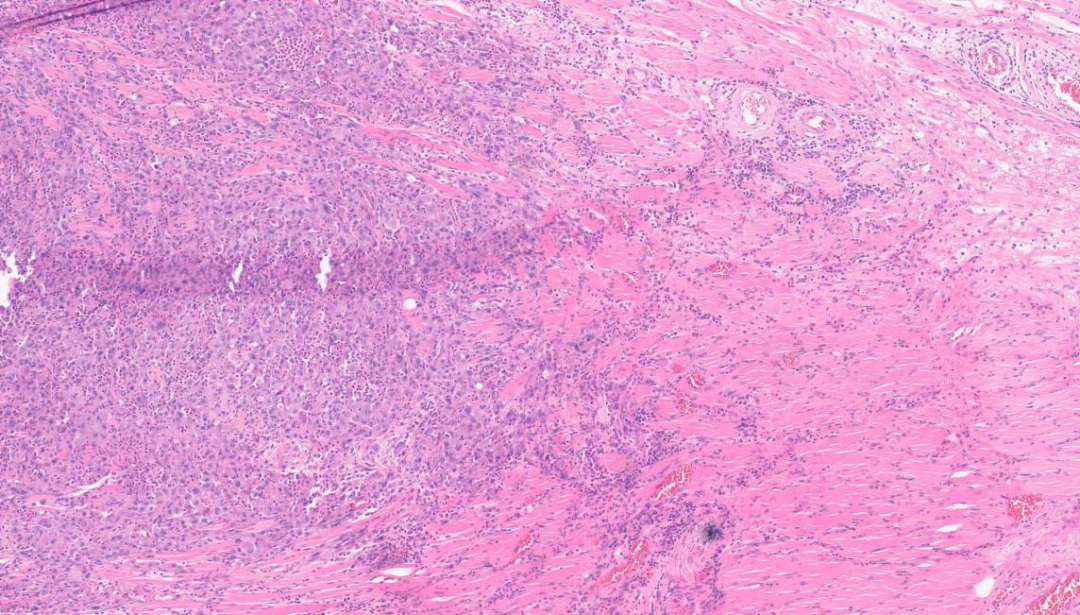
肿瘤累及横纹肌
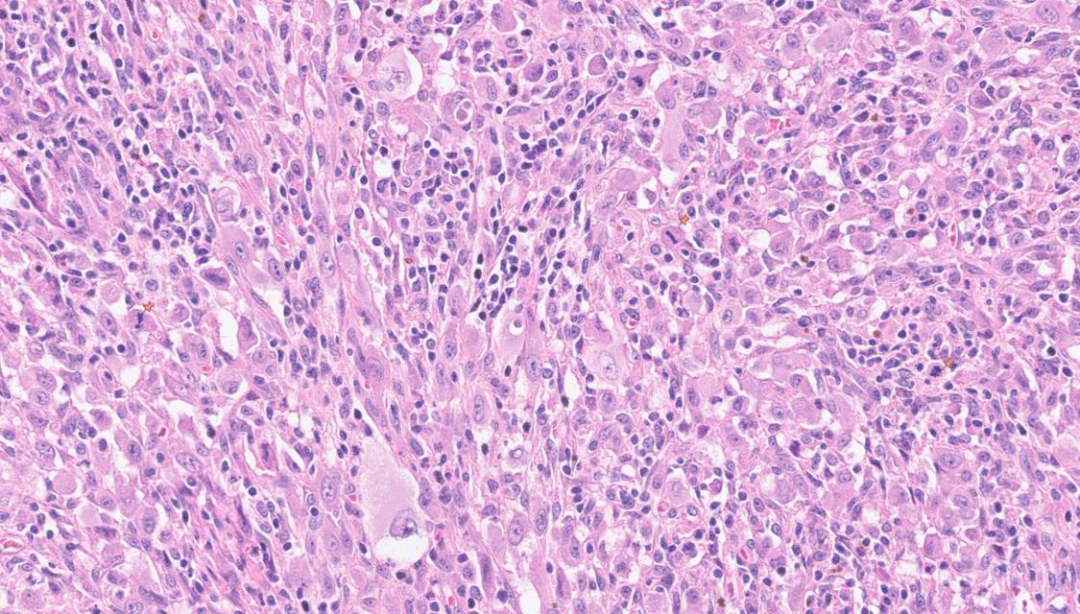
实性区细胞显著异型
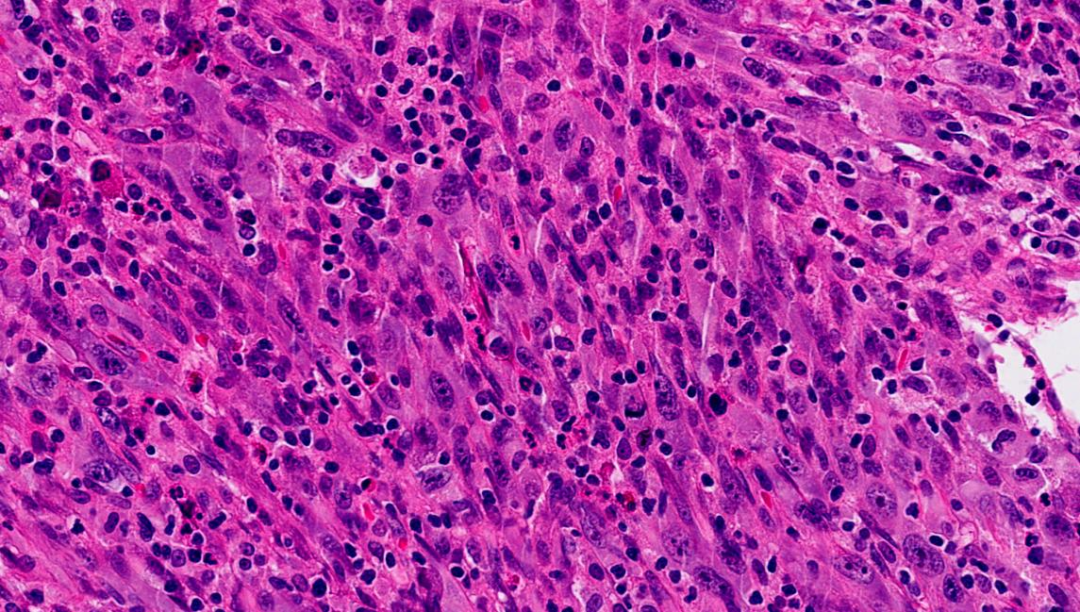
部分肿瘤细胞呈梭形
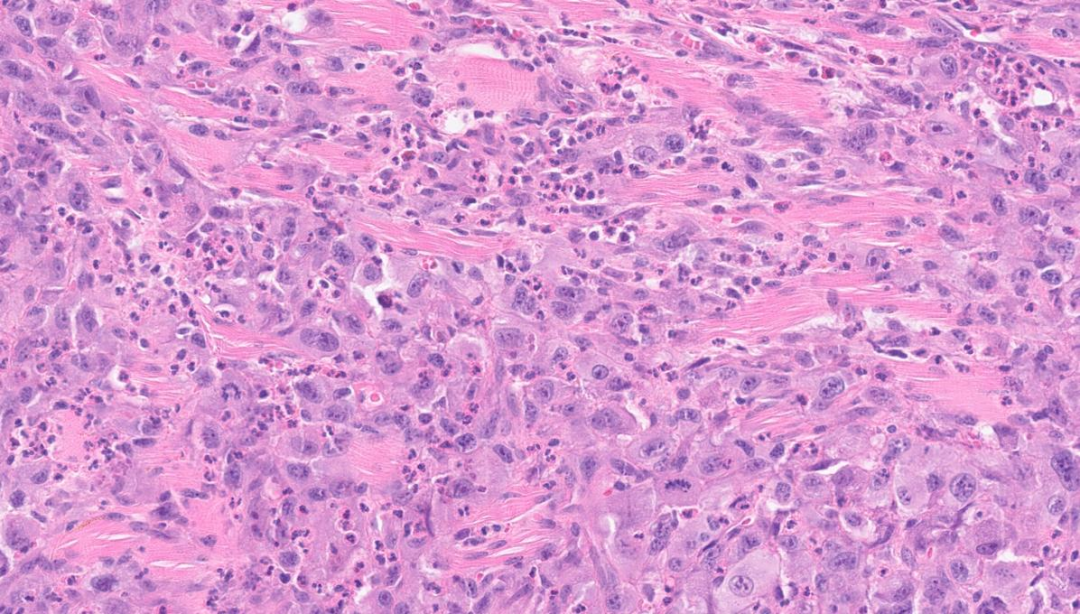
伴中性粒细胞浸润
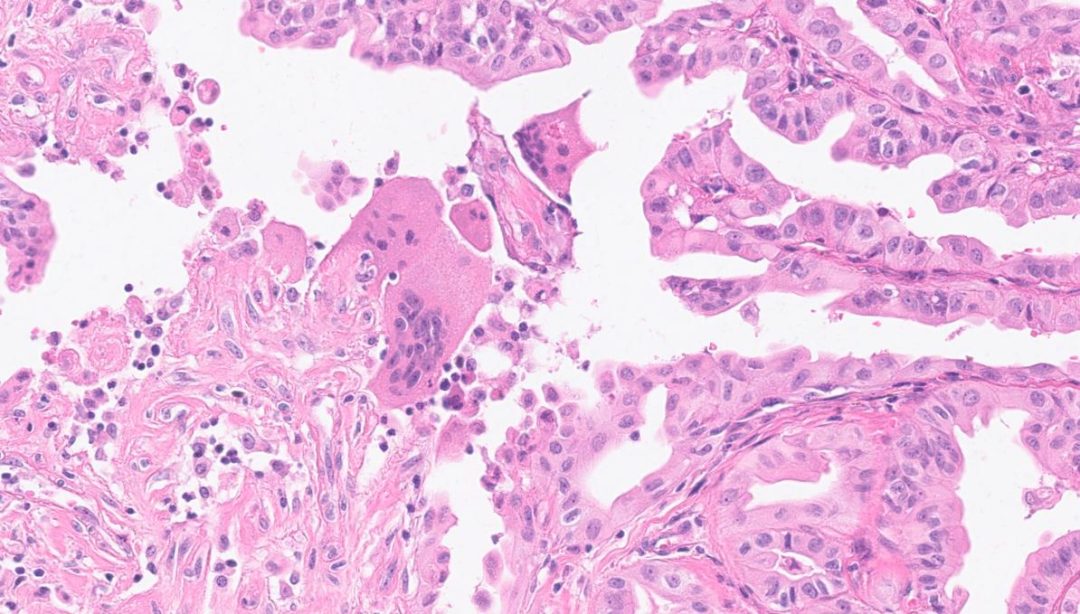
可见破骨样巨细胞
免疫组化
阳性标记
1.瘤细胞 AE1/AE3+(非弥漫)
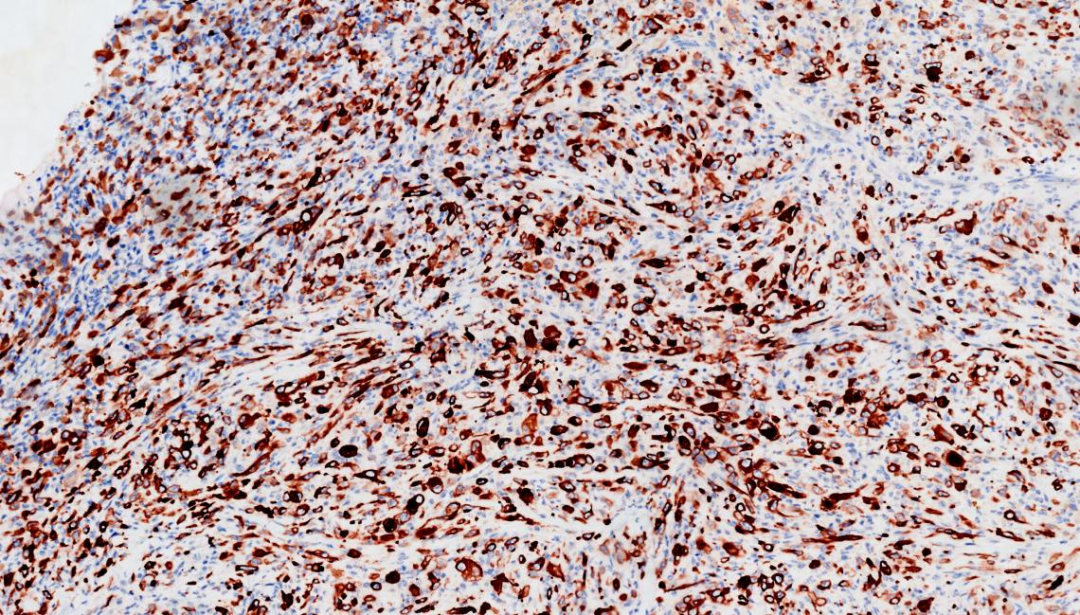
AE1/AE3,阳性率低于分化型甲状腺癌
2.CK19点灶+
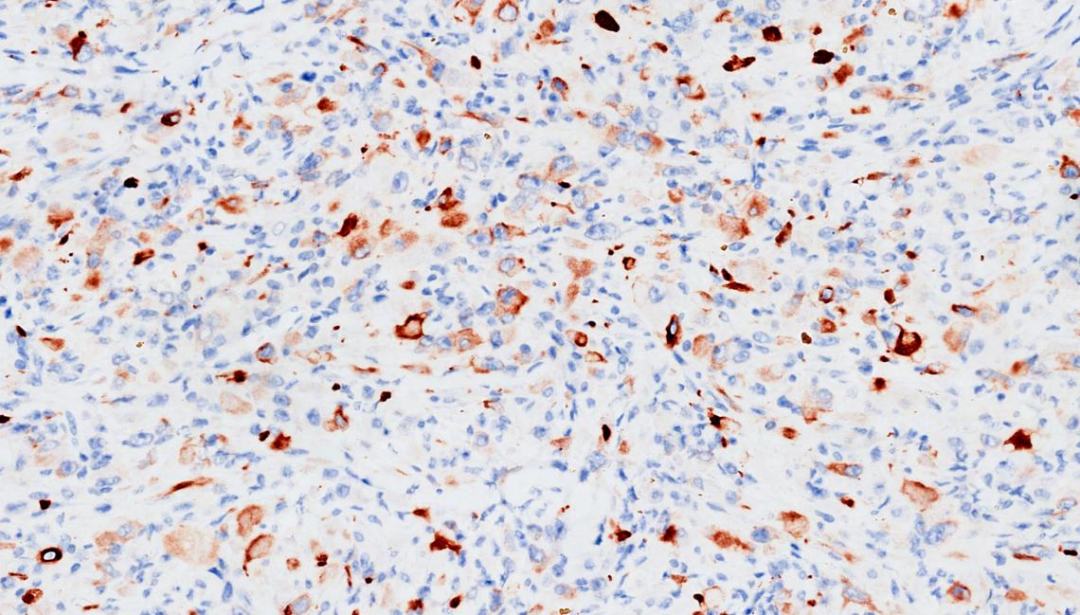
CK19
3.Vimentin+
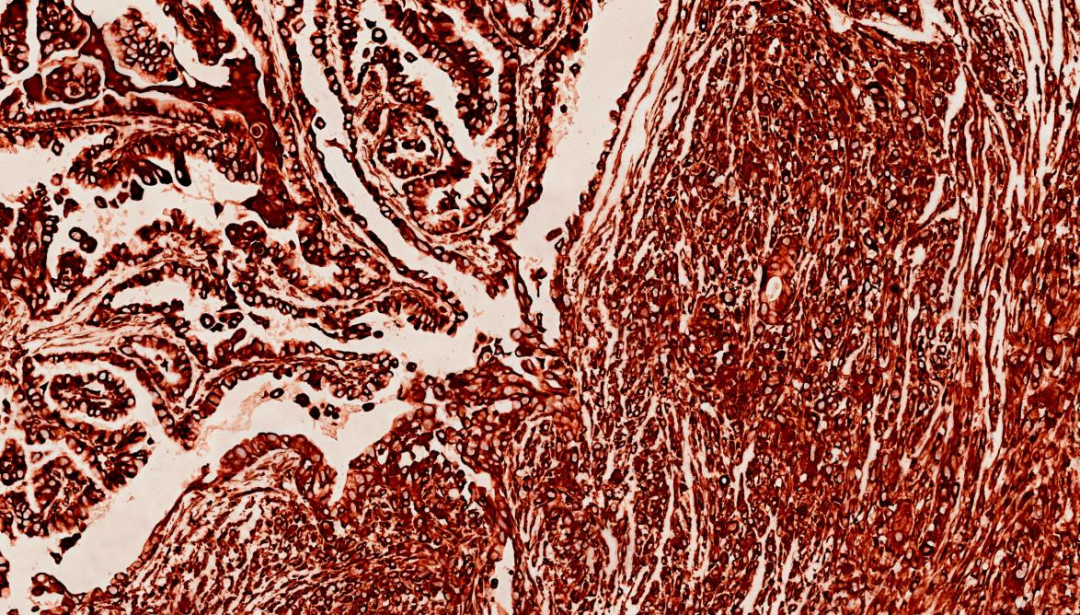
Vimentin
4.PAX-8+
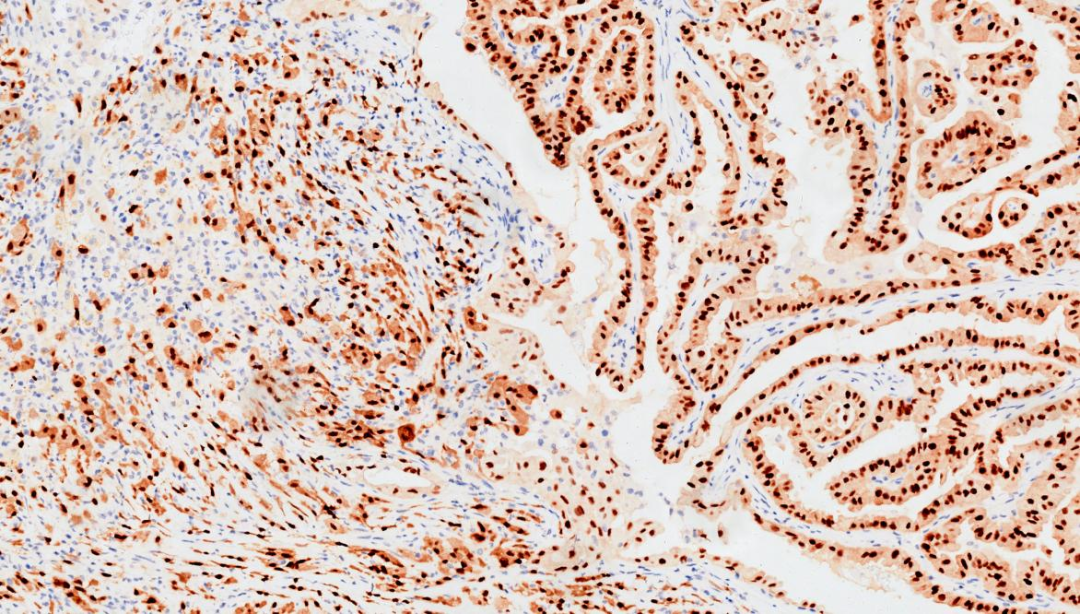
PAX-8
5.乳头状区域TG+
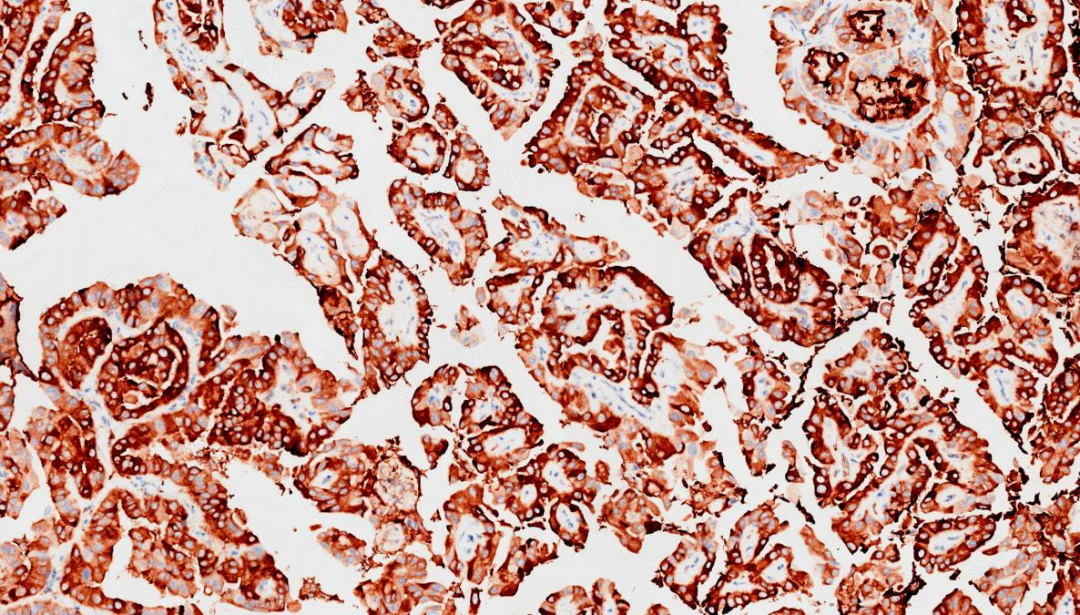
TG,乳头状区域
6.乳头状区域 HBME-1+

HBME-1,乳头状区域
7.Ki67 乳头状区域约5%,实性区约30%
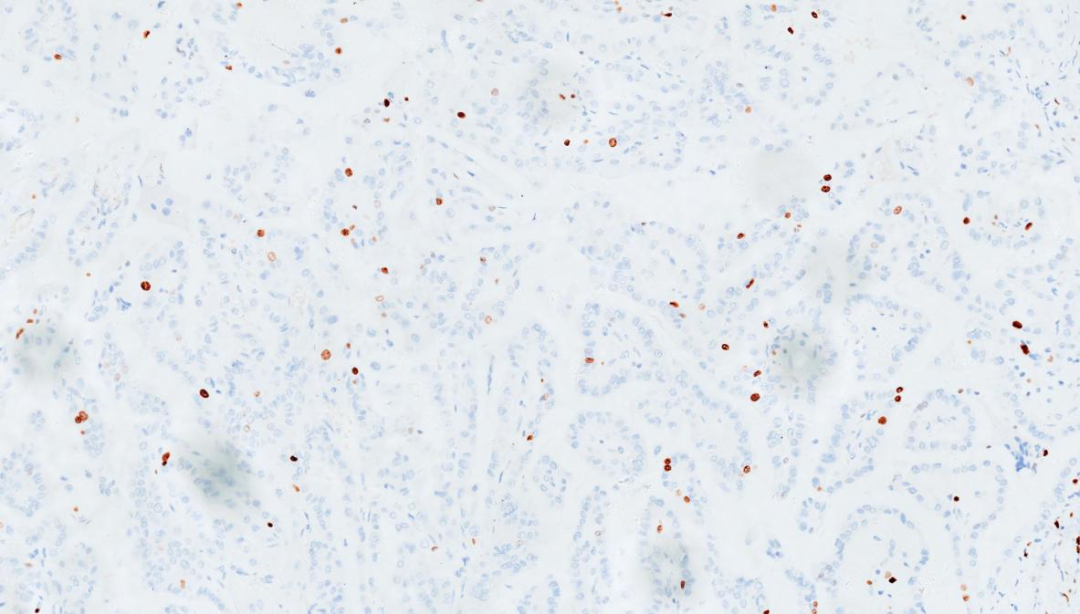
Ki67,乳头状区
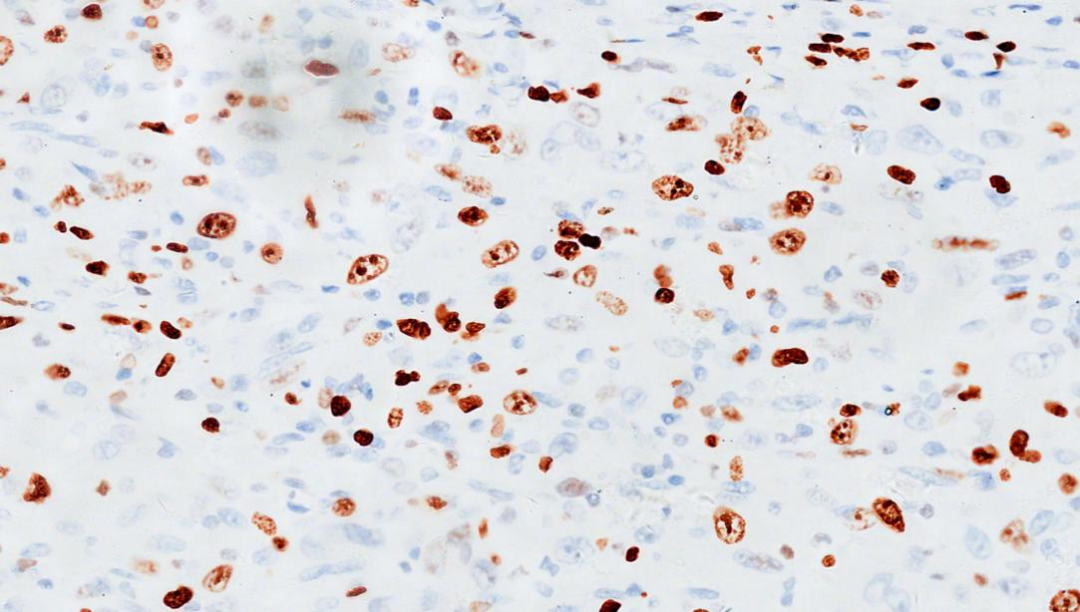
Ki67,实性区
阴性标记
1.实性区瘤细胞 TG-
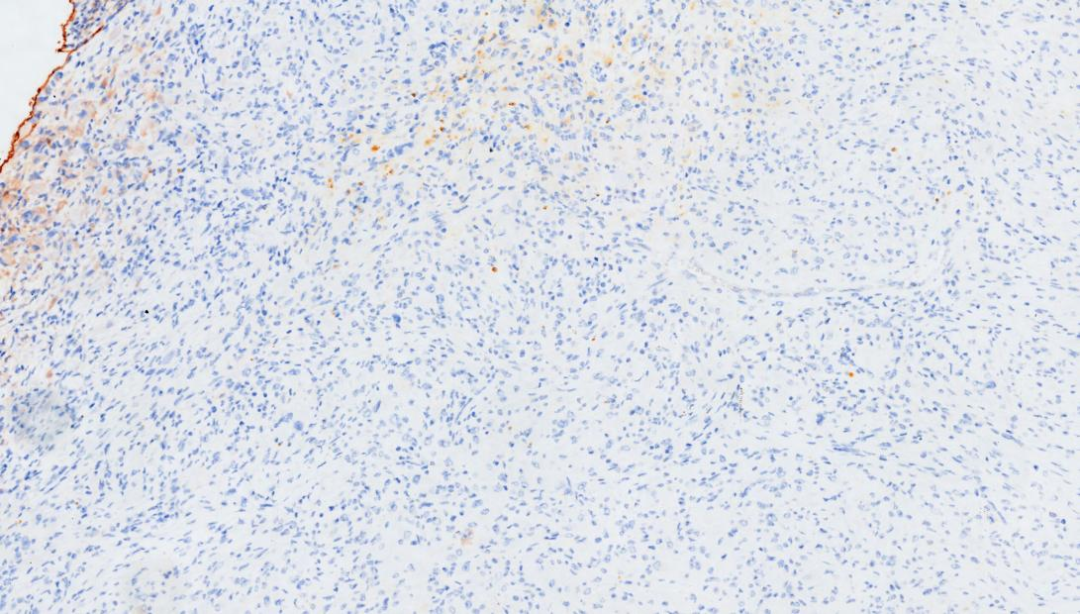
TG,实性区
2.实性区瘤细胞HBME-1 -
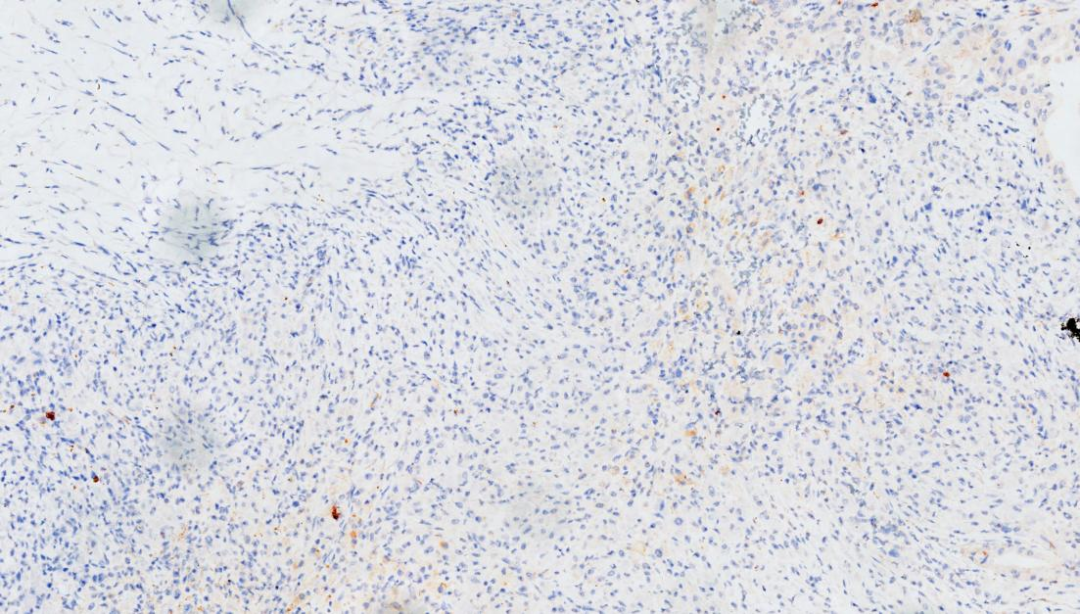
HBME-1,实性区
免疫组化结果汇总
阳性标记:
乳头状区:Vimentin+;AE1/AE3弥漫+,CK19弥漫+,P53(野生型),TG+,TTF-1+,PAX-8+,HBME-1+,EGFR+,Ki67 5%;
实性区:Vimentin+,AE1/AE3+,CK19+,P53(野生型),TG-,TTF-1+,PAX-8+,HBME-1-,EGFR+,Ki67 30%。
阴性标记:
PGM-1(-),P63(-),ALK-D5F3(-),CD21(-),CD23(-)。
分子检测
具有较强或潜在临床意义的基因变异(包括 I 类及 II 类):
-
PIK3CA H1047R
-
TERT 228G>A
-
BRAF V600E
最终诊断
“左颈大块”恶性肿瘤,侵犯横纹肌,符合甲状腺乳头状癌(高细胞亚型),其中伴有间变性癌成分。
定义
间变性甲状腺癌(ATC)
ICD-O 8020/3
又称未分化癌,是一种罕见的高度侵袭性恶性肿瘤,约占甲状腺肿瘤的2%~3%。进展迅速,预后极差,多数患者在1年内死亡。甲状腺间变性癌除局部浸润外,常伴局部淋巴结或远处转移。
临床特点
流行病学:
地方性甲状腺肿地区(缺碘),间变性甲状腺癌的发生率较高。病人通常是老年人,男女比例为2:1。
主要症状:
声音嘶哑和呼吸、吞咽困难,约30%引起声带麻痹。
治疗:
所有ATC都是IV期肿瘤,由于肿瘤转移迅速,几乎无法进行根治性手术。但仍建议尽可能切除局部病灶。术后需辅助放化疗,但I131治疗通常无效。
组织形态
1.细胞形态
①肉瘤样:以恶性梭形细胞为主,与高级别多形性肉瘤相似
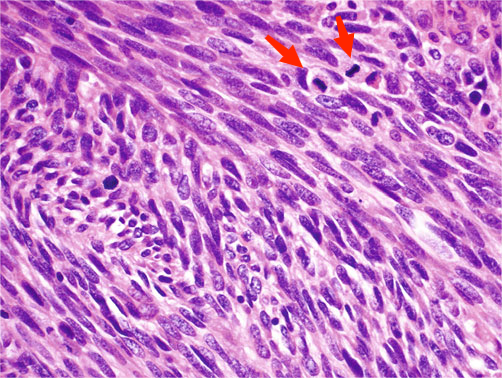
②巨细胞型:由高度多形性的肿瘤细胞组成,可见多核瘤巨细胞

③上皮样型:紧密排列的鳞样或鳞状瘤巢,有丰富的嗜酸性胞浆;偶有角化。
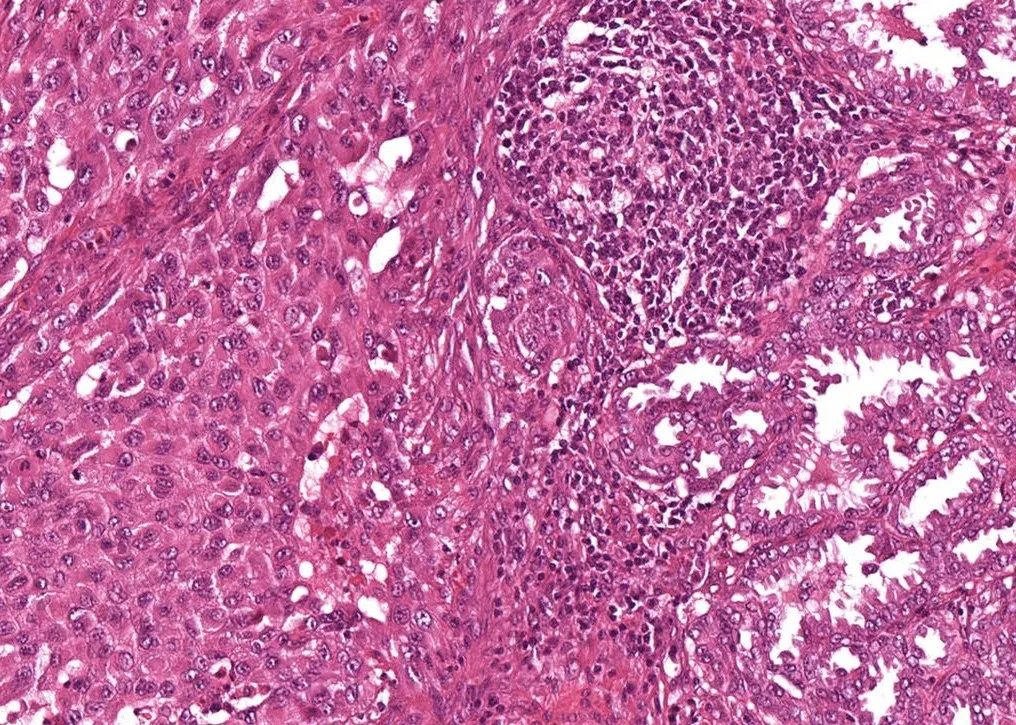
2.伴随现象
①中性粒细胞浸润
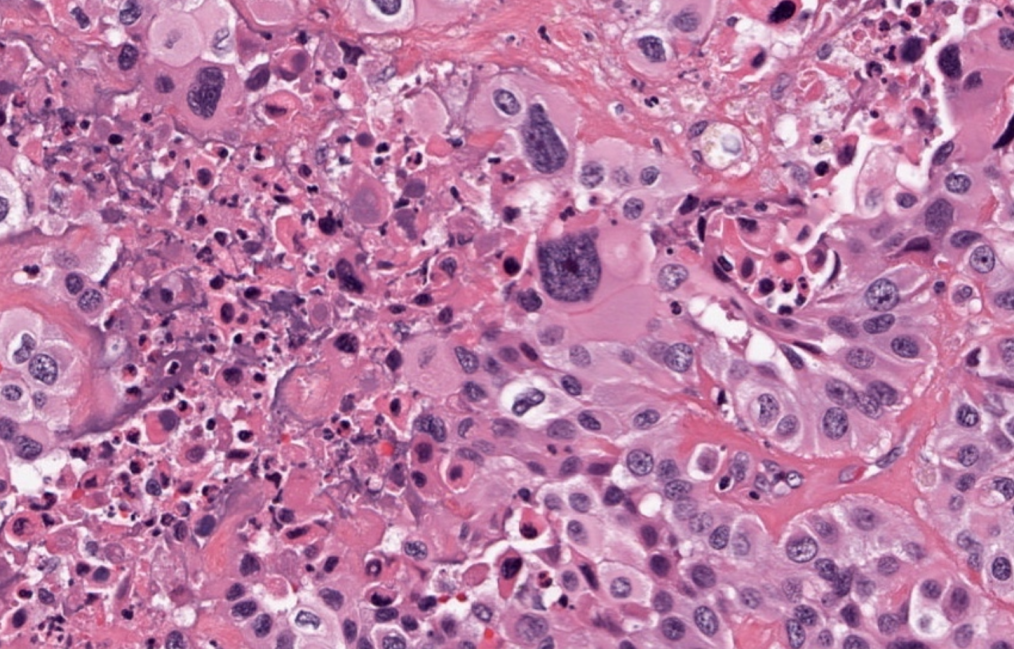
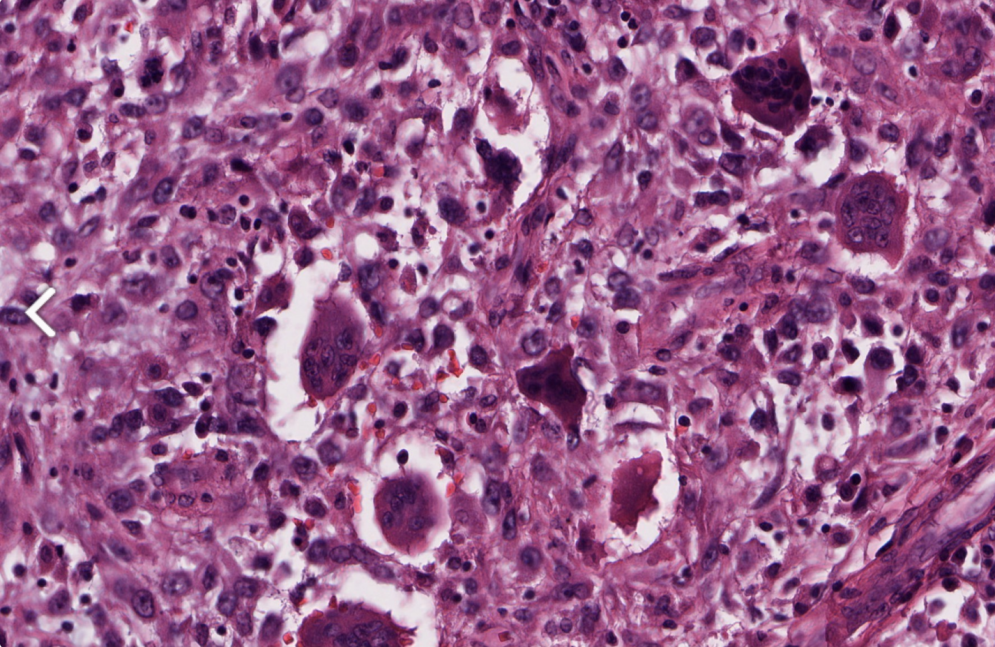
②破骨样巨细胞
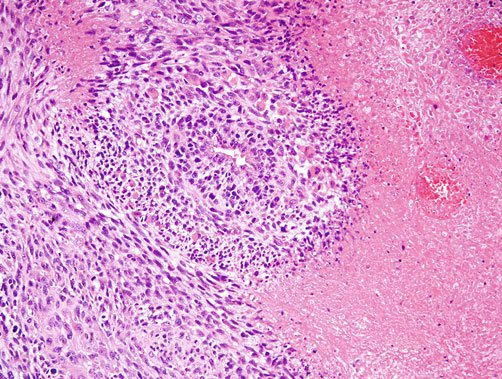
③凝固性坏死
3.少见亚型
①寡细胞型ACT
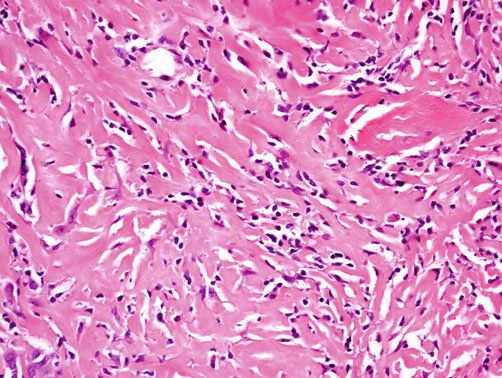
于纤维背景中可见少量异型梭形细胞
②横纹肌样ACT
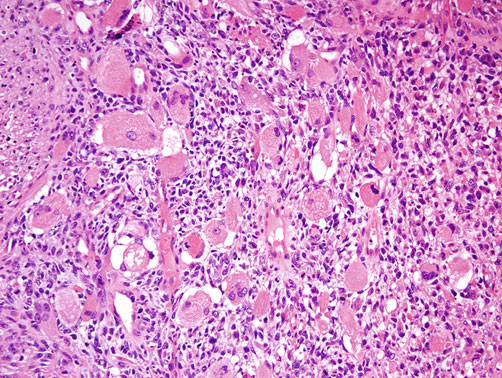
肿瘤细胞呈横纹肌细胞样形态
③鳞状细胞型:第五版WHO中,原先的甲状腺鳞状细胞癌被归为间变性甲状腺癌的一种亚型。
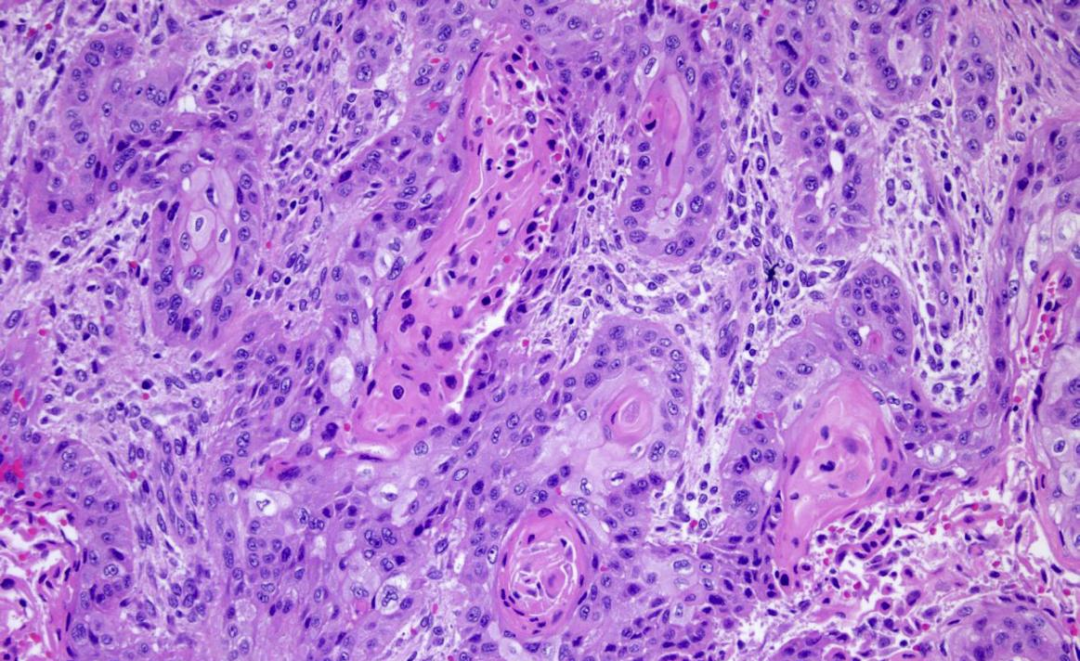
肿瘤局灶或弥漫性鳞状表型
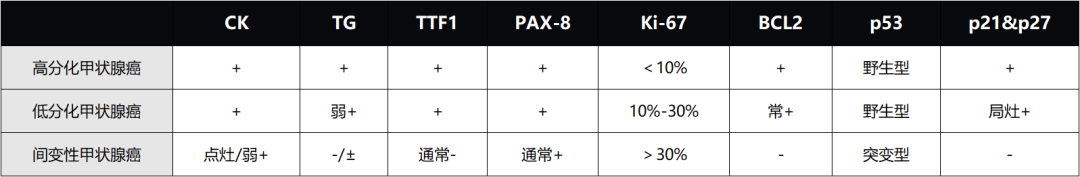
免疫组化
常用的免疫组化标记如下表,间变性甲状腺癌TG、TTF-1常阴性,但PAX-8通常保留。同时Ki67>30%且p53呈突变型。
分子改变
分子改变分为两个阶段:早期改变和晚期改变
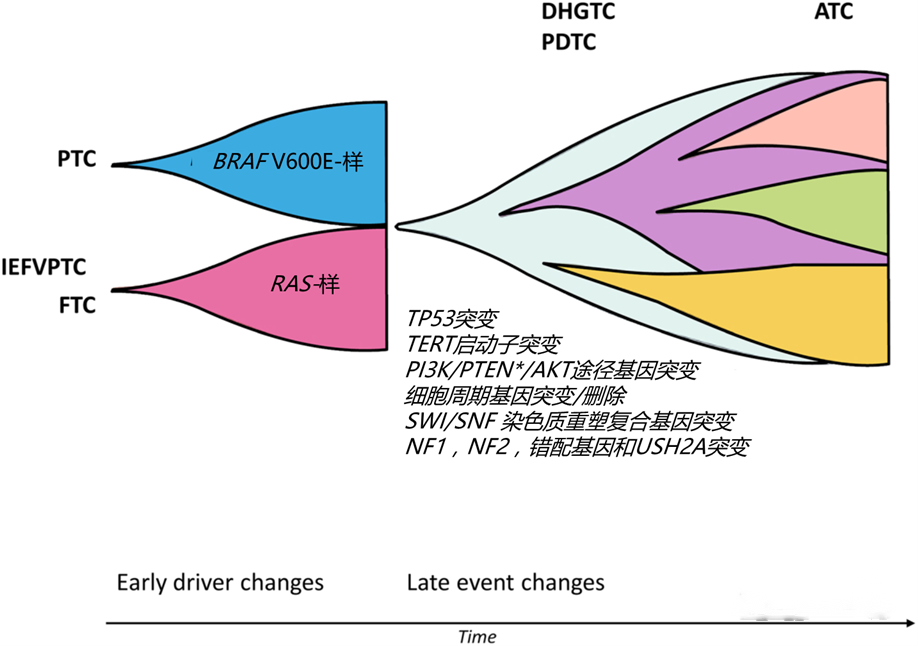
甲状腺癌分子改变的两个阶段
早期改变:
以RAS和BRAF基因突变为主,主要影响肿瘤的分化方向
RAS基因:
RAS基因编码的p21蛋白位于细胞膜内侧,对GTP和GDP有高度亲和力和较弱的GTP酶活性,从而以类似G蛋白偶联的方式激活信号通路,促进细胞增殖。在甲状腺肿瘤中,RAS突变主要与滤泡状生长的肿瘤(滤泡性癌、滤泡亚型乳头状癌等)相关。
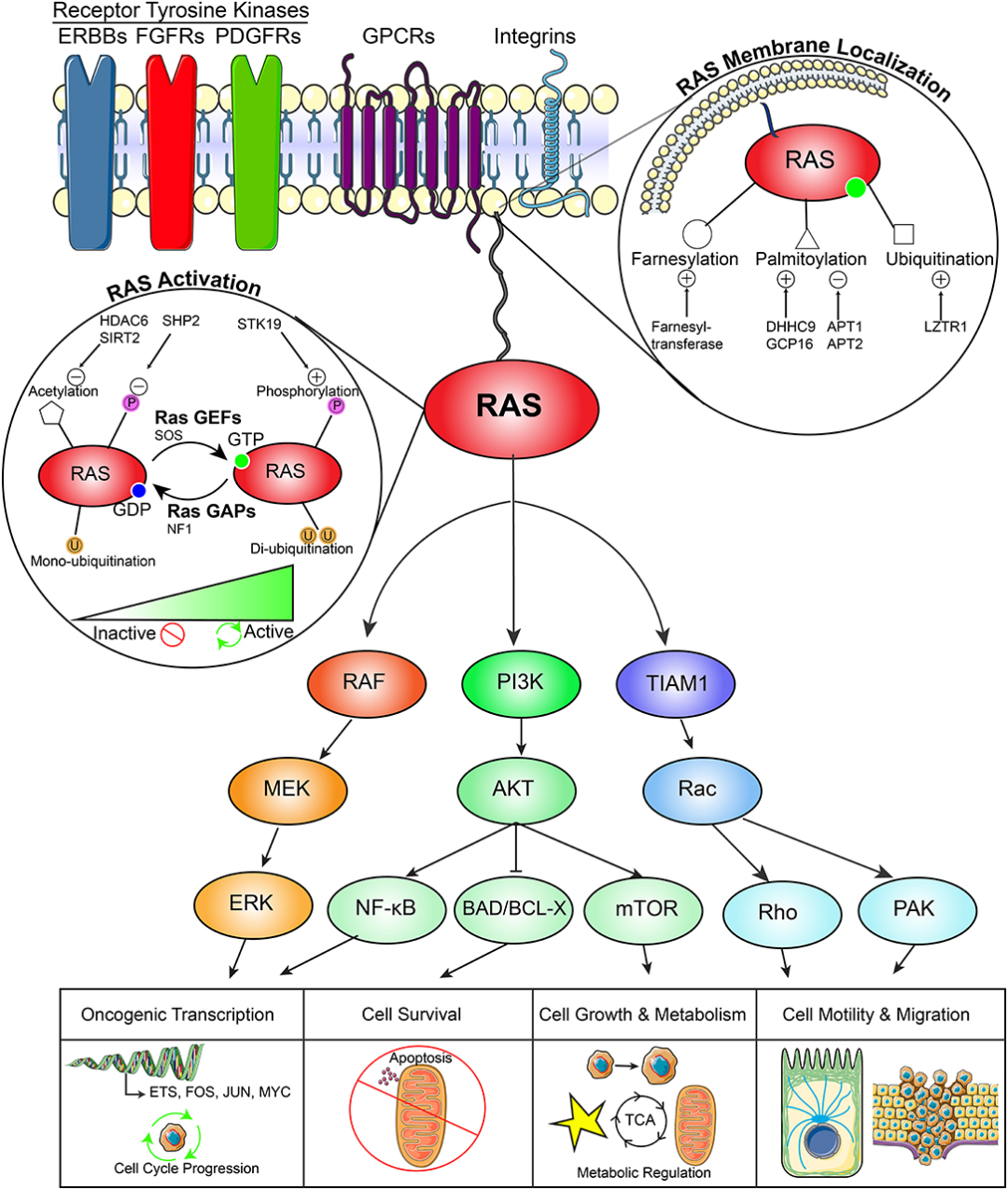
RAS通路作用机制
BRAF基因:
BRAF基因编码MAPK-ERK通路中的RAF激酶。生长因子与细胞表面的受体(EGFR)结合后,受体通过RAS激酶发出信号。RAF蛋白是活化的RAS蛋白的直接效应子,并进一步激活下游的MEK、ERK等信号分子,最终促进细胞增殖。V600E是BRAF基因最常见的突变位点,在甲状腺肿瘤中,BRAF突变主要与乳头状癌相关。
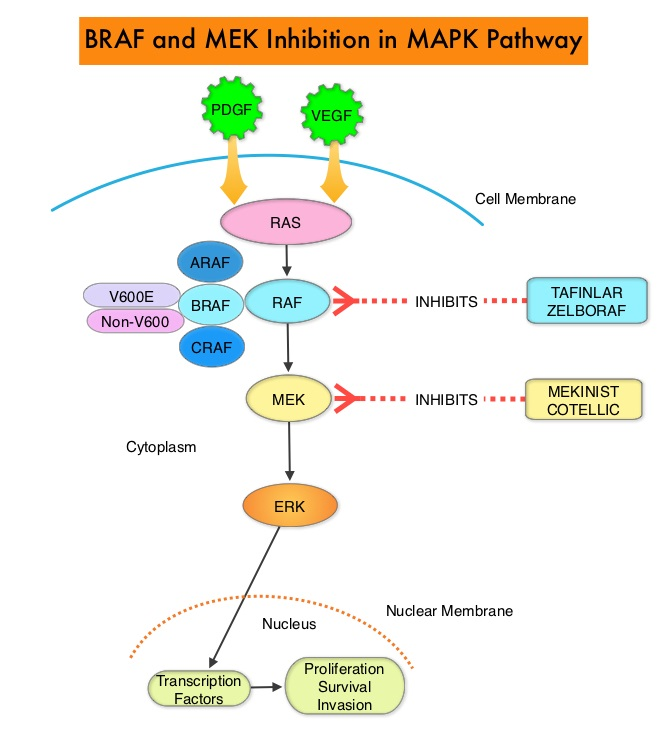
BRAF通路作用机制
晚期改变:
以TERT启动子和p53基因突变为主,主要影响肿瘤的恶性程度
TERT基因:
TERT基因编码端粒酶逆转录酶,TERT的异常上调可使染色体保持其端粒长度而持续扩增。TERT启动子突变是预后不良的有力标志,当TERT启动子与BRAF V600E或RAS共突变时,预后最差。
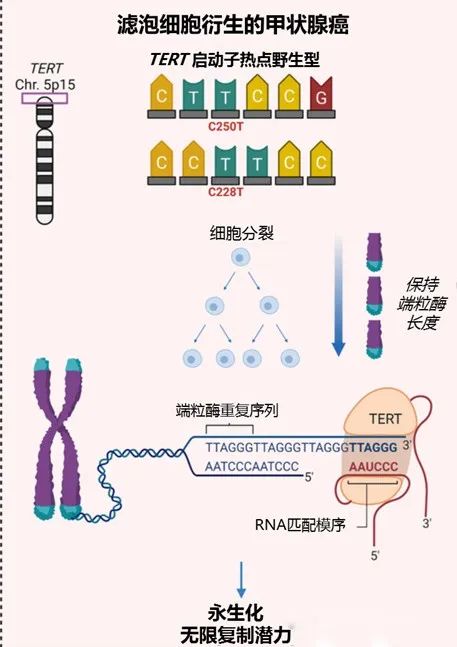
TERT基因的作用机制
p53基因:
p53基因是人体重要的抑癌基因。其编码的p53蛋白可在细胞DNA损伤时抑制细胞生长周期,使之停留于G1/S的节点,以提供充裕的时间进行修复。并在DNA无法修复时激活凋亡程序。在甲状腺肿瘤中,超过50%的间变性癌存在p53基因突变,是有力的诊断依据。
鉴别诊断
1.血管肉瘤
通常血管肉瘤表达内皮细胞相关标记,如CD31、CD34、ERG、Fli1等,而间变性甲状腺癌表达上皮标记物,如AE1/AE3。但两者均可出现上皮/内皮标记的异常表达,此时可用甲状腺特异性标记物,如PAX-8进行鉴别。
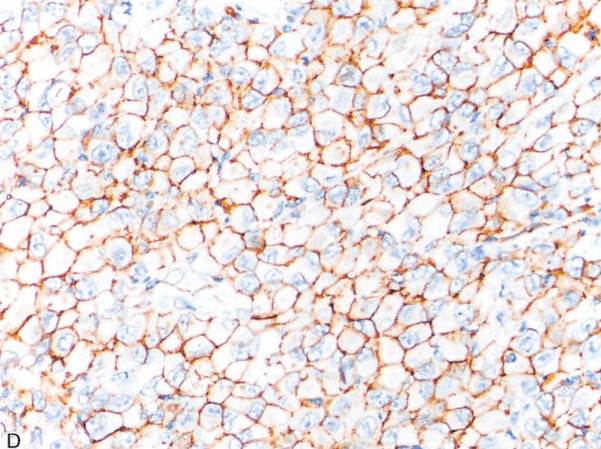
上皮样血管肉瘤,表达AE1/AE3
2.低分化甲状腺癌
低分化甲状腺癌(PDTC)形态学和行为上介于分化(滤泡和乳头状)癌和间变性癌之间。诊断标准依据都灵共识包括以下四项:
(1)按普通标准诊断滤泡性甲状腺癌;
(2)实性、小梁或岛状的生长方式;
(3)缺乏甲状腺乳头状癌的经典核特征;
(4)至少具有以下三个特征之一:
①核膜不规则(“葡萄干样”),无核内假包涵体;
②每2mm2(约10HPF)中≥3个核分裂;
③具有肿瘤性坏死。
与ATC相比,PDTC中肿瘤细胞异型程度和有丝分裂活性相对较低,并不具备间变性癌的组织学特征。此外PDTC大部分留有TG表达,可用以进行鉴别。
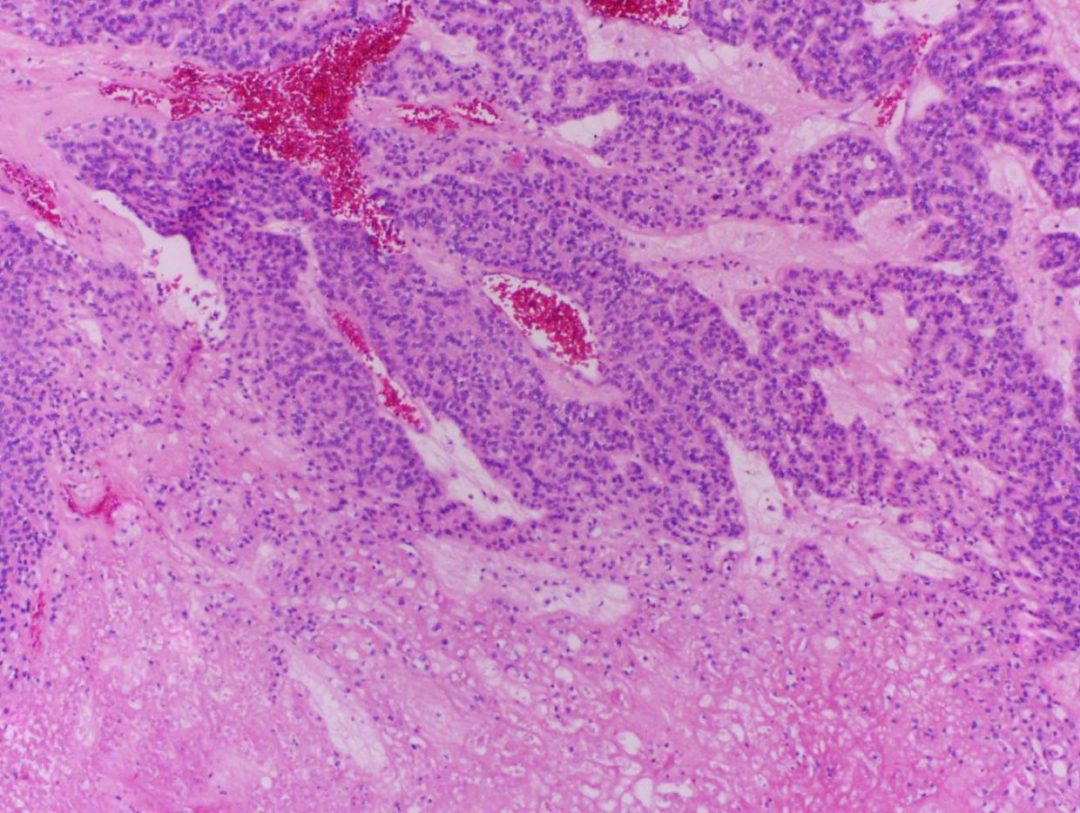
低分化甲状腺癌,梁状生长模式
3.甲状腺髓样癌
甲状腺髓样癌(MTC)呈现甲状腺C细胞分化证据,镜下可见淀粉样沉积物和“盐与胡椒粒(salt & pepper)”样染色质。
免疫组化降钙素+可用以区分具有间变特征的MTC和ATC。
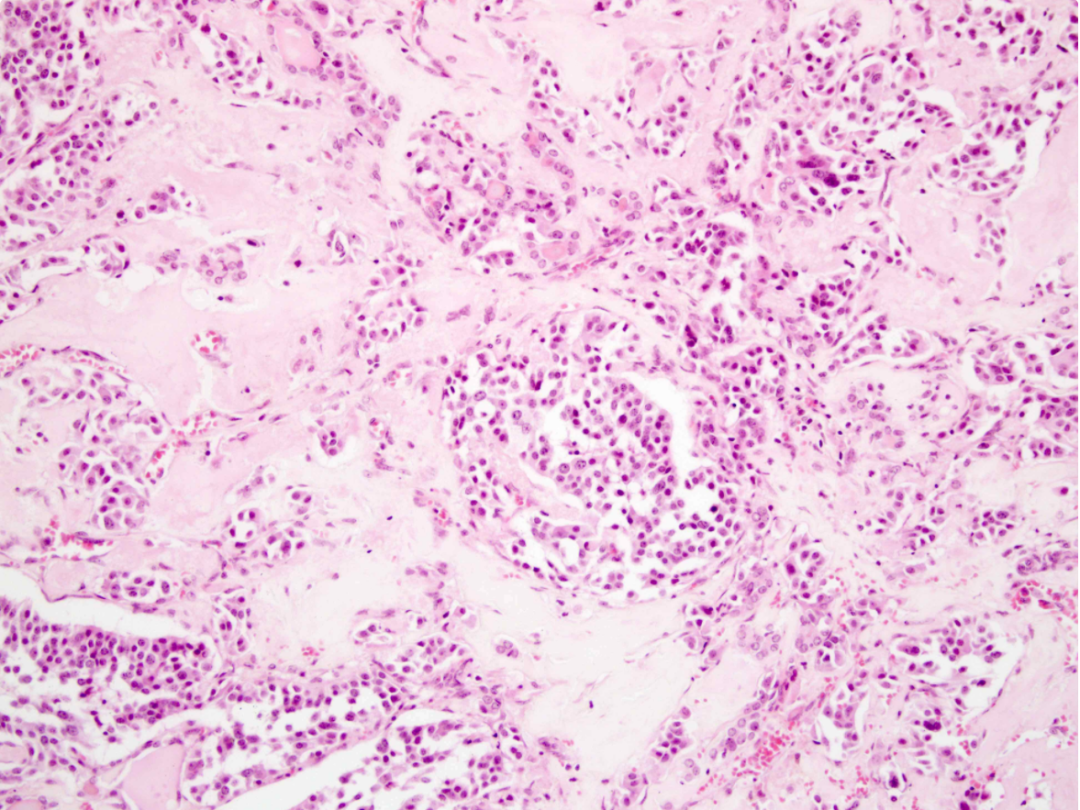
甲状腺髓样癌,可见淀粉样沉积物
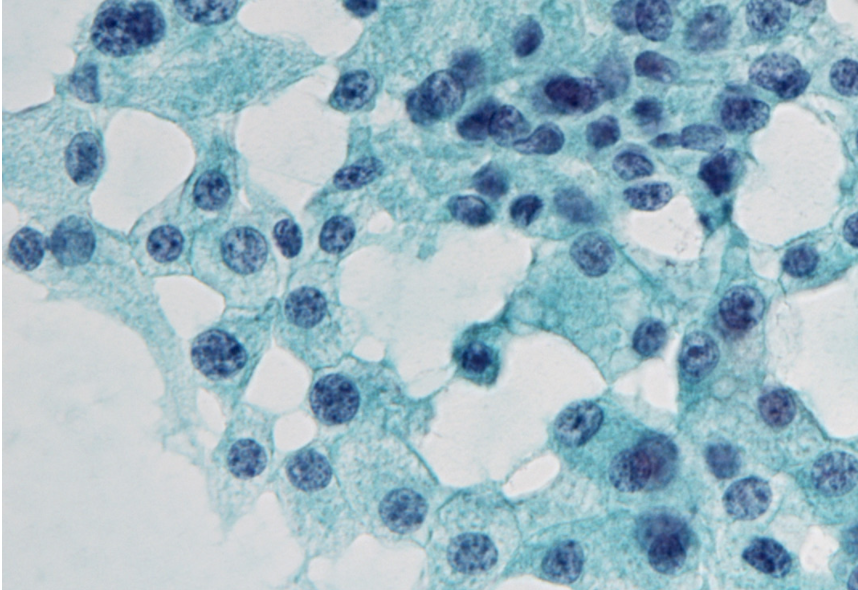
“盐与胡椒粒”样染色质
4.Riedel甲状腺炎
Riedel甲状腺炎是一种以纤维化为主要特征的炎症过程,需与寡细胞型ACT鉴别。
Riedel甲状腺炎患者血清多可查到抗甲状腺抗体,同时病变较为局限,伴慢性炎症细胞浸润,且间质中上皮性标志物阴性。

Riedel甲状腺炎,可见大量慢性炎症细胞浸润
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#甲状腺癌# #间变性甲状腺癌#
69