Clin Cancer Res:遗传发育所等发现儿童急性淋巴细胞白血病发病的表观遗传新机制
2019-01-28 佚名 遗传与发育生物学研究所
中国科学院遗传与发育生物学研究所鲍时来团队通过检测上百例儿童B系前体细胞急性淋巴细胞白血病(BCP-ALL)患者的骨髓样品,发现蛋白质精氨酸甲基转移酶家族成员PRMT5的表达量及其修饰的组蛋白H4R3的对称性双甲基化(H4R3sme2)水平显着升高。
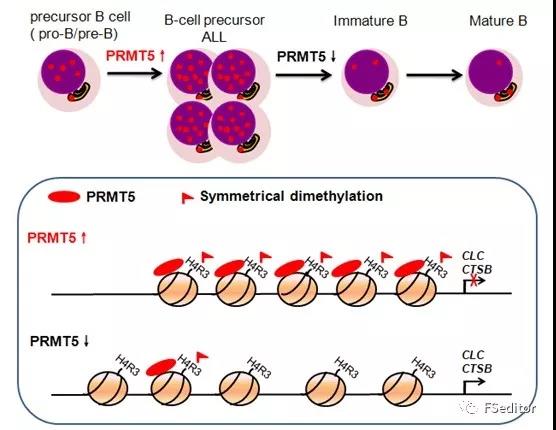
PRMT5及H4R3sme2水平异常升高导致BCP-ALL的机制模式图(图片来源于网络)
儿童急性淋巴细胞白血病(ALL)是儿童最常见的恶性肿瘤性疾病,位居儿童疾病致死率之首。淋巴细胞分化受阻是白血病重要的表型。但是,导致儿童白血病淋巴细胞分化障碍的发病机理目前还不清楚。
中国科学院遗传与发育生物学研究所鲍时来团队通过检测上百例儿童B系前体细胞急性淋巴细胞白血病(BCP-ALL)患者的骨髓样品,发现蛋白质精氨酸甲基转移酶家族成员PRMT5的表达量及其修饰的组蛋白H4R3的对称性双甲基化(H4R3sme2)水平显着升高。疾病缓解后PRMT5及H4R3sme2水平显着下降。在B系前体淋巴细胞白血病的细胞中降低PRMT5的表达不仅能够促进白血病细胞的凋亡,而且促进白血病细胞向B淋巴细胞谱系的下游分化;而在成熟的B淋巴细胞中高表达PRMT5能够使其去分化到未成熟阶段。
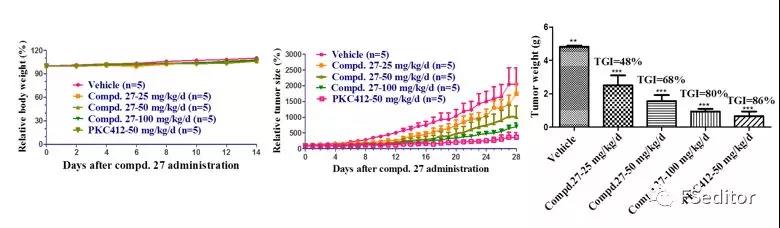
为了进一步研究PRMT5的体内功能以及其异常表达是否能导致ALL,鲍时来研究组通过制作小鼠骨髓移植模型,发现移植了高表达PRMT5的骨髓细胞后,受体小鼠骨髓细胞中pro-B细胞占B系细胞的比例显着升高,而其下游各个分化阶段的B系细胞的比例均显着下降,表明PRMT5的升高促使B系细胞分化阻滞在pro-B细胞阶段,这与临床中BCP-ALL的表型相一致。该研究首次报道PRMT5表达的异常升高及其H4R3的异常甲基化是儿童ALL中的普遍现象。
这种异常造成疾病是由于PRMT5及组蛋白异常的高甲基化导致PRMT5下游靶基因CLC和CTSB的沉默,进而抑制B系前体细胞向成熟细胞的分化。这些研究表明,H4R3sme2和PRMT5作为白血病的敏感的表观遗传生物标志物,不仅可用于白血病的诊断和预后评估,还将成为开发新的治疗白血病药物的靶点,对实现诱导白血病细胞向正常细胞分化有重要意义。
研究结果于1月12日在线发表在Clinical Cancer Research 杂志上。鲍时来研究组梅玫、北京儿童医院郑胡镛研究组张瑞东为论文的共同第一作者。该研究得到中科院先导专项、国家自然科学基金、北京市医院管理局“登峰”人才计划和首都卫生发展科研专项项目的支持。
原始出处:Mei Mei, Ruidong Zhang, Zhongwei Zhou, et al. PRMT5-mediated H4R3sme2 confers cell differentiation in Pediatric B-cell Precursor Acute Lymphoblastic Leukemia. Clin Cancer Res. January 11, 2019
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#淋巴细胞白血病#
71
#淋巴细胞#
57
#发育#
117