Sci Trans Med:癌症免疫疗法或可治疗艾滋病
2019-08-14 赵熙熙 中国科学报
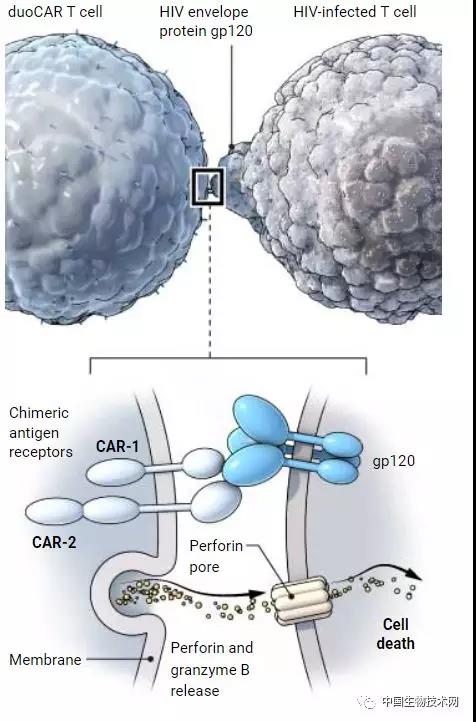
药物在控制艾滋病病毒(HIV)方面效果惊人的好,但并非对所有人都有效,也并非没有副作用。这也就是为什么一小部分被称为精英控制者的患者长期以来吸引研究人员的原因——前者的免疫系统能够在没有药物的情况下自然抑制HIV达几十年之久。如今,一个研究团队受到老鼠实验的启发,希望为HIV感染者提供专门针对这种病毒的免疫细胞,从而在临床上创造出精英控制者。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#TRA#
47
#Med#
47