JAMA:90%以上宫颈癌可预防!关注宫颈癌筛查的6大临床进展
2024-01-03 医学新视点 医学新视点 发表于上海
该综述详细阐述了人乳头瘤病毒(HPV)与宫颈癌发生的病理机制、HPV感染癌变的高危因素、HPV疫苗接种、筛查建议、异常结果处理、宫颈癌的治疗和预后等内容,以期为临床预防宫颈癌提供参考。
子宫颈癌是常见的妇科恶性肿瘤之一,发病率在中国妇科恶性肿瘤中居第二位,仅次于乳腺癌。中国子宫颈癌患者中位发病年龄为51岁,但主要好发于2个年龄段,以40~50岁为最多,60~70岁又有一高峰出现,且近年来平均发病年龄逐渐降低,有年轻化趋势。世界卫生组织(WHO)在2020年发布了《加速消除子宫颈癌全球战略》,得到了全球多个国家的响应和支持。
近期,《美国医学会杂志》(JAMA)发表宫颈癌筛查综述,详细阐述了人乳头瘤病毒(HPV)与宫颈癌发生的病理机制、HPV感染癌变的高危因素、HPV疫苗接种、筛查建议、异常结果处理、宫颈癌的治疗和预后等内容,以期为临床预防宫颈癌提供参考。

截图来源:JAMA
HPV与宫颈癌
目前,已经明确高危型HPV持续感染是宫颈癌及癌前病变发生的必要因素,即宫颈癌发生癌变的过程中,HPV感染是最为重要的环节。宫颈的鳞状上皮和柱状上皮交接处易受HPV感染致癌的影响,宫颈癌病变通常发生于此。此外,新的证据表明,储备细胞容易发生恶变,也是HPV感染的“潜伏处”。
HPV演变和致癌性
HPV是个庞大的病毒“家族”。根据病毒基因遗传差异可逐级分为属、物种、类型、变异谱系和亚系。HPV可分为5个属:α-、ν-、μ-、β-和γ-属,导致宫颈癌的主要是α-HPV。
α-HPV又细分为α-1、α-2……α-14等14个物种,其中α-9、α-7、α-5和α-6物种含有致癌的HPV基因型,称为“高危型”。α-9物种的HPV基因型几乎都致癌,如HPV-16、HPV-31、HPV-33、HPV-35、HPV-52和HPV-58,其中HPV-16致癌性最强,超过60%的宫颈鳞状细胞癌和腺癌、口咽癌和其他生殖器癌均与其相关,而其他α-9物种的HPV基因型具有中度致癌风险。α-7物种中HPV-18和HPV-45与鳞状细胞癌和腺癌相关。
α-7物种中HPV-39、HPV-59、HPV-68以及α-5物种中HPV-51以及α-6物种中HPV-56致癌风险均较低。低风险HPV基因型与宫颈癌风险增加无关,其检测结果在癌症筛查预防方面无显著价值。
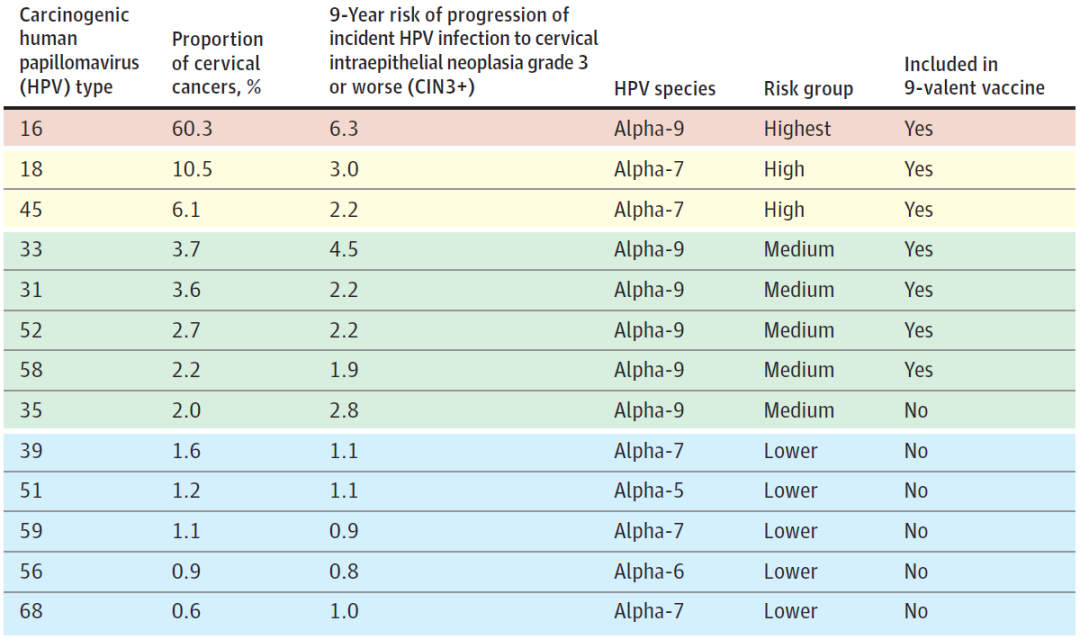
▲致癌的HPV类型(图片来源:参考文献[1])
通常,若临床检查发现HPV-16或HPV-18时,建议做阴道镜检查;若临床检查发现HPV-16或HPV-18以外基因型阳性结果,则需要结合患者情况来判断是否需要做阴道镜检查。目前,针对其他基因型(称为“扩展基因分型”)的临床管理指南也正在制定中。
HPV感染活动期和潜伏期
无论哪种基因型,只要有新的HPV感染,都被认为是可产生新病毒拷贝的活动性HPV感染,这期间宫颈可能无/有明显改变,病理检查宫颈细胞存在可疑或轻微异常,但一般没有癌前病变。由于体内免疫系统的作用等原因,大多数感染在12~24个月内会自然消失,80%的女性HPV感染为一过性。虽然有研究表明,自然感染后可获得免疫力,但目前对这方面的了解知之甚少,不过比较明确的是,接种HPV疫苗获得的免疫力至少可维持15年。
HPV感染可持续存在于宫颈基底细胞中并缓慢复制,这个过程称为“潜伏感染”。在潜伏感染期间,宫颈阴道HPV检测结果为阴性,癌变风险最低。
HPV感染5年内复发率高达15%,因此HPV检测结果为阳性有两种可能:1)新感染;2)旧感染复发,但目前临床检测无法区分。不过,无论是新发还是复发感染,5年内进展为癌前病变的风险大约为3%,所以也没有区分二者的必要。
HPV感染持续存在和进展为癌前病变
HPV持续感染是宫颈癌及癌前病变发生的必要因素。所谓“癌前病变”,指的是被感染的细胞从复制性感染到克隆生长的变化。目前,已经确定了几种癌前病变相关生物标志物,如从复制性感染到癌变期间,可观察到病毒和宿主DNA标志物甲基化。美国FDA批准了一种用于检测细胞转化的技术——p16/Ki67双染技术,p16和Ki67联合表达,则提示HPV感染可引起细胞转化。
侵袭:鳞状细胞癌和腺癌
HPV基因型决定了HPV感染后进展为癌前病变和癌症的可能性,HPV-16基因型的癌变风险最高。腺癌是宫颈内膜腺细胞癌症,几乎所有的腺癌均由HPV-16、HPV-18和HPV-45引起。腺癌与鳞状细胞癌的病理生理并不相同,鳞状细胞癌起源于外表皮的鳞状细胞。
由于筛查和阴道镜检查都存在漏查腺癌癌前病变的可能,因此腺癌癌前病变的检出率和治疗率都低于鳞状细胞癌,在筛查预防癌变方面,效果不如鳞状细胞癌。
HPV感染癌变的高危因素
女性一生中,感染高危型HPV的概率高达70%以上,但仅有不到10%的女性会最终发展为宫颈癌或宫颈上皮内瘤变。这是因为除了持续性高危型HPV感染外,还需要其他因素共同参与和作用,才会最终引起宫颈癌。引发宫颈癌的的危险因素可分为2大类:1)生物学因素,即高危型HPV持续感染;2)外源性的行为性危险因素。
由于HPV主要通过性传播,所以一些可能增加HPV感染的因素,如性卫生不良、多个性伴侣等都可能增加HPV感染风险,从而增加罹患宫颈癌的风险。据统计,大多数性活跃人群一生都有HPV感染,但具体的占比情况并不明确。
《宫颈癌诊疗指南(2022年版)》指出:月经及孕产因素、吸烟、口服避孕药、自身免疫性疾病或者长期免疫抑制剂、营养不良/营养失调等原因也可能增加癌变风险。
HPV疫苗接种
接种HPV疫苗有助于预防HPV感染、癌前病变和癌症。现行指南建议:所有儿童,不分性别,在9岁时均可接种疫苗,13岁之前间隔6~12个月接种2剂HPV疫苗;13~26岁未接种疫苗者应接种疫苗;15岁及以上开始接种疫苗者,建议接种3剂。
疫苗主要作用为预防,因此首次性交后,疫苗有效性会有所下降。大多数研究显示,14岁前接种疫苗获益最大,随着年龄的增加,接种疫苗的有效性会逐渐降低。建议27~45岁的个体在接种疫苗前与临床医师共同决策。
宫颈癌筛查建议
有效的筛查和治疗癌前病变,可将宫颈癌终身风险降低到0.5%以下。建议无症状个体定期筛查,以早期诊断和治疗癌前病变,预防宫颈癌的发生。需要说明的是,筛查仅适用于无症状的个体,若出现疑似宫颈癌症状,如不规则出血、疼痛或阴道分泌物,需要进行包括盆腔检查和宫颈细胞学检查措施在内的相关评估。
筛查注意事项
有效的宫颈癌筛查包含以下步骤:
1)评估筛查的必要性,仅在有筛查指征时开展筛查。
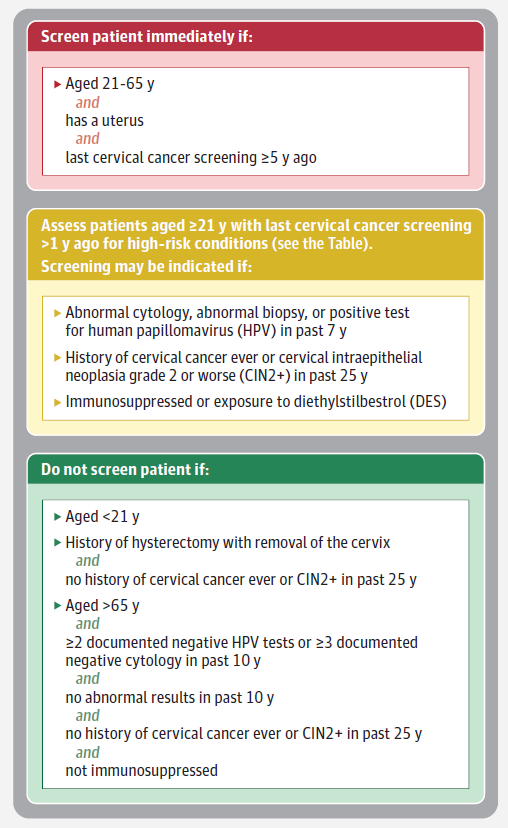
▲评估筛查需求(图片来源:参考文献[1])
2)使用HPV检测(无论是否有细胞学检查)进行筛查。细胞学检测癌前病变敏感性为50%~70%,而HPV检测敏感性超过90%,因此,相比于单独的细胞学检测,HPV检测结果阴性更能说明患者无癌前病变。若后续HPV筛查结果均为阴性,则癌症风险持续降低。此外,97%的癌前病变患者HPV检测结果为阳性,从这个角度看,同时进行HPV检测和细胞学检测能带来的额外帮助比较有限。
筛查年龄
30岁左右罹患宫颈癌的风险就开始增加。因此,建议年龄在25~65岁有子宫颈的个体,至少每5年进行一次筛查。
美国预防服务特别工作组建议:年龄在21~29岁人群仅采用细胞学检查进行筛查;年龄在30~65岁可单独进行细胞学检查或细胞学检查联合HPV检测。
美国癌症协会公布的最新指南则建议:年龄25~65岁的人群,每间隔5年单独进行HPV检测【见上图红色框内容】。
监测或高风险人群
通常普通人群筛查后约20%个体属于高风险筛查人群,他们既往有异常结果、既往有癌前病变或使用免疫抑制剂,需要每隔1~3年筛查一次【见上图黄色框内容】。
停止筛查
不建议对以下无症状患者进行筛查:1)年龄<21岁;2)无宫颈者(如子宫切除术后),除非先前已诊断为宫颈癌或癌前病变;3)年龄>65岁且符合停止筛查要求【见上图绿色框内容】。
宫颈癌筛查结果异常怎么办?
子宫颈上皮内病变包括:
-
低级别鳞状上皮内病变(LSIL),即子宫颈上皮内瘤病变1级(CIN1)
-
高级别鳞状上皮内病变(HSIL),包括子宫颈上皮内瘤病变2级和3级(CIN2和CIN3)
-
高级别腺上皮内病变(HG-CGIN),也称原位腺癌(AIS)
HSIL以及AIS为子宫颈癌前病变。癌前病变风险判断有助于临床医生明确对当前或既往筛查结果异常患者的下一步管理策略。根据“同等风险,同等管理”原则,美国阴道镜与子宫颈病理学会(ASCCP)推荐以CIN3及以上病变风险作为主要临床终点,用以明确个体是否需要做阴道检查或是可以安全地在1年、3年或5年内进行重复HPV检测或联合检测。
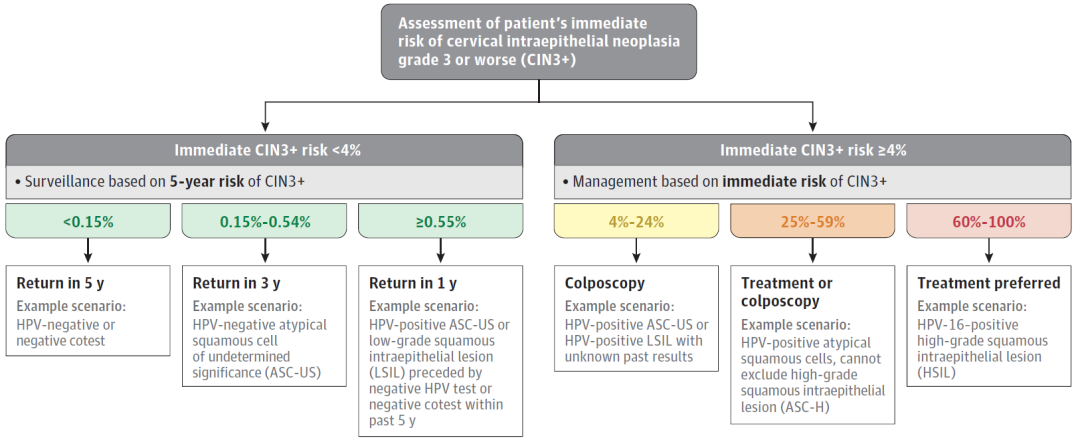
▲风险管控、临床措施和患者场景示例(图片来源:参考文献[1])
此外,对于筛查结果异常的患者,可能还需要使用阴道镜和病理活检来明确癌前病变,以及时采取治疗措施,阻止癌症发展。
宫颈癌治疗及预后
癌前病变的治疗除了消除阴道镜检查发现的病变外,可能还需要切除或消除整个鳞状上皮和柱状上皮交接处组织,目的是消除大部分已经发生癌前转化的HPV感染细胞,降低宫颈癌发生风险。治疗方式包括电切、消融等。
在电切或消融后,CIN3在6个月时短期复发风险分别为1.6%和2.9%,第12个月时复发风险会上升到3.2%和7.2%。在癌前病变治疗后几十年内,浸润性癌症的风险依然会升高,特别是年龄50岁以上的患者。因此,指南建议每隔3年筛查一次,直到65岁;治疗后至少25年内,只要患者身体健康,就可以选择继续治疗。
小结
在美国,每年大约有10万人接受宫颈癌前病变治疗,以预防宫颈癌的发生。有宫颈的人群应进行HPV检测,若结果为阳性,则需要进行细胞学检测和明确HPV基因型,以评估宫颈癌前病变风险,确定后续是否需要接受阴道镜检查和治疗。青春期时接种HPV疫苗,有助于预防90%以上的宫颈癌前病变和癌症的发生。
参考资料
[1]Perkins RB, Wentzensen N, Guido RS, et al. Cervical Cancer Screening: A Review. JAMA. 2023 Aug 8;330(6):547-558. doi: 10.1001/jama.2023.13174. PMID: 37552298.
[2]中华人民共和国国家卫生健康委员会. 宫颈癌诊疗指南(2022年版). http://www.nhc.gov.cn/yzygj/s7659/202204/a0e67177df1f439898683e1333957c74/files/361f086b71214c4e8336fa7d251dc020.pdf
[3]中国优生科学协会阴道镜和子宫颈病理学分会,中华医学会妇科肿瘤学分会,中国抗癌协会妇科肿瘤专业委员会,等. 中国子宫颈癌筛查指南(一). 中国妇产科临床杂志. 2023, 24(4): 437-442 https://doi.org/10.13390/j.issn.1672-1861.2023.04.029
[4]于艳芳,魏芳.人乳头瘤病毒致宫颈癌变机制研究进展[J].中国生育健康杂志,2021,32(3):298-3011.DOI:10.3969/j.issn.1671-878X.2021.03.025.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#HPV# #宫颈癌# #人乳头瘤病毒#
89