Nature Nanotechnology:新靶点+新载体:黎松团队通过siRNA联合化疗,增强抗肿瘤免疫反应
2022-12-01 “生物世界”公众号 “生物世界”公众号 发表于上海
肿瘤细胞中的促翻转酶(scramblase)Xkr8在铂类化疗药物治疗后显著高表达,并基于此开发了一种能共载铂类化疗药物和Xkr8-siRNA的新型纳米载体——PMBOP-CP。
乒乓球是中国的国球,为中国带来了无数的荣誉,想要打好乒乓球,正确运用球拍两面的正胶与反胶是其中关键,这样才能精确控制乒乓球的运动轨迹和旋转方向。
有趣的是,癌细胞也深谙“乒乓绝技”,它们通过翻转细胞膜的磷脂酰丝氨酸(phosphatidylserine,PS),在细胞膜上产生类似于“正胶与反胶”的效果,以此应对免疫系统的疯狂“扣杀”。因此,如果我们能控制癌细胞膜上的PS的翻转,就能开发出一种新型癌症免疫疗法,为广大癌症患者带来新的希望。
2022年11月24日,美国匹兹堡大学黎松教授团队联合卢斌峰教授在 Nature Nanotechnology 期刊发表了题为:Targeting Xkr8 via nanoparticle-mediated in situ co-delivery of siRNA and chemotherapy drugs for cancer immunochemotherapy 的研究论文。
该研究发现,肿瘤细胞中的促翻转酶(scramblase)Xkr8在铂类化疗药物治疗后显著高表达,并基于此开发了一种能共载铂类化疗药物和Xkr8-siRNA的新型纳米载体——PMBOP-CP。该载体在体内能高效靶向肿瘤细胞、阻断磷脂酰丝氨酸(PS)翻转,显著抑制结肠癌和胰腺癌模型中的肿瘤生长。


黎松教授
该论文的通讯作者黎松教授表示,这项研究与两个创新之处:一个是发现了新的治疗靶点,另一个是开发了新的纳米载体,这种纳米载体在在免疫疗法和化疗药物的选择性递送方面非常有效。这项研究令人兴奋,因为它具有很高的转化价值和应用潜力。
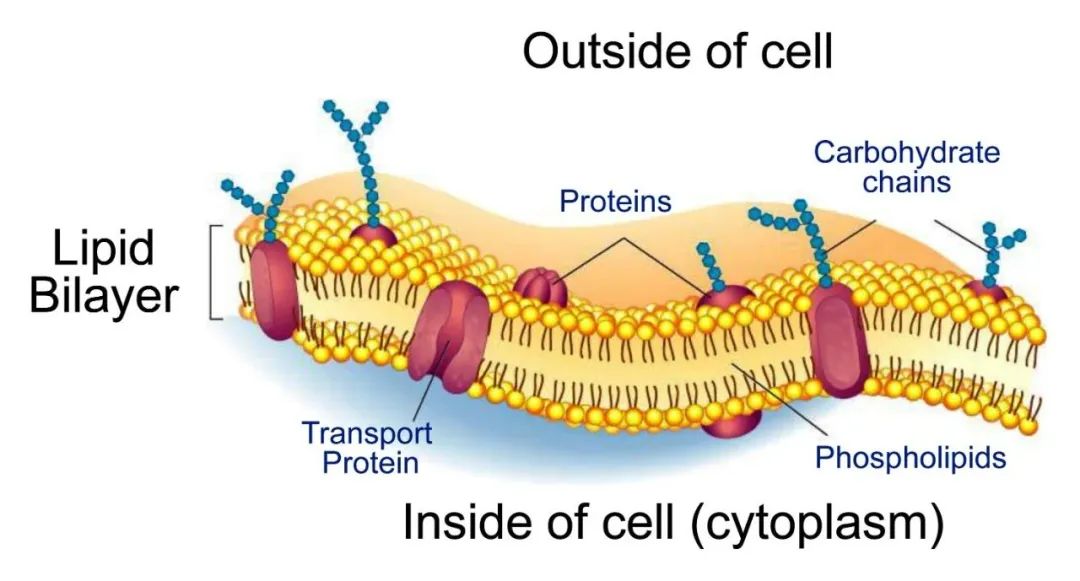
磷脂酰丝氨酸(PS)是一类普遍存在于哺乳动物细胞中的磷脂,作为膜结构的重要组成部分,PS通常仅分布于细胞膜磷脂双分子层的内侧。然而,在细胞凋亡过程中,内侧的PS会被暴露在磷脂双分子层的外侧,这个由内而外的翻转过程依赖PS促翻转酶(scramblase)——Xkr8。
值得注意的是,在癌症治疗过程中,常规放化疗会使PS在肿瘤细胞凋亡时被Xkr8不可逆地外翻。外翻的PS会与免疫细胞上的受体结合,引起严重的免疫抑制,从而使得放化疗的临床效果大打折扣。因此,抑制Xkr8或许是一种改善肿瘤微环境、达到更好治疗效果的新途径。
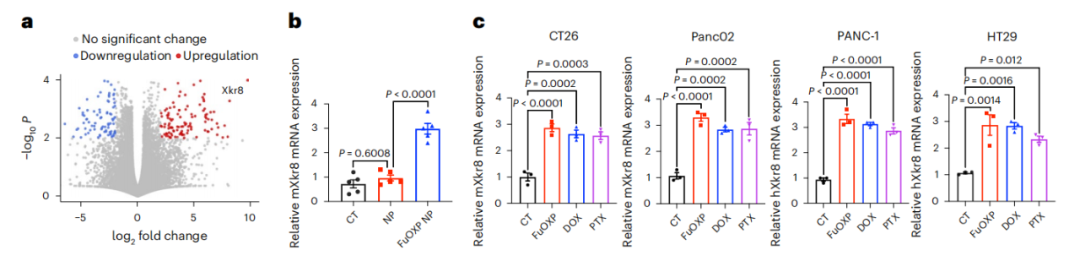
在这项最新研究中,研究团队首先发现,经铂类化疗药物治疗后,癌细胞系和小鼠肿瘤中的促翻转酶Xkr8在转录和蛋白水平上均显着增加。由于目前尚无Xkr8的小分子抑制剂,研究人员开发了一种新型纳米载体PMBOP-CP,用于小鼠肿瘤模型中Xkr8-siRNA和铂类药物(FuOXP)的共递送。
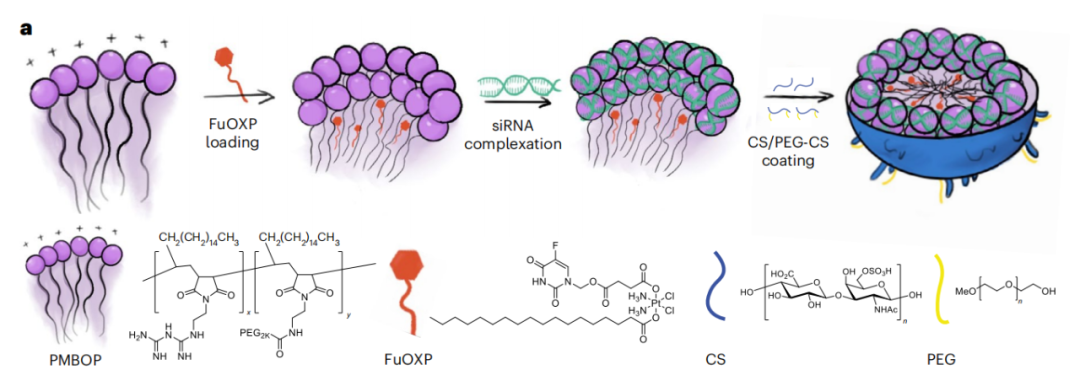
PMBOP聚合物具有两亲性:其脂质链能帮助铂类药物更有效地加载到疏水核心中,并促进聚合物与细胞膜的融合;其阳离子双胍基团能增强与siRNA形成的离子相互作用,从而使siRNA稳定地结合在聚合物表面。
众所周知,具有阳离子表面的药物载体不适合全身递送到远处实体肿瘤。因此,为了适用于静脉注射,研究团队还是用了带有大量负电的硫酸软骨素(CS)和聚乙二醇化-CS(PEG-CS)的混合物包覆PMBOP聚合物表面,最终形成了PMBOP-CP纳米载体。
值得一提的是,CS是CD44(在各类肿瘤细胞及肿瘤内皮细胞上有很高的表达)的一种重要天然配体。通过调节PMBOP、CS和PEG-CS的比例,不仅可以中和载体表面的正电荷,还能精准靶向肿瘤细胞。
新型纳米载体——PMBOP-CP的制备流程
基于上述提到的这些要点,研究团队通过一系列的筛选确定了PMBOP-CP纳米载体各组分的最优比例,在静脉给药后,小鼠肿瘤中铂的浓度随着时间的推移而增加,且肿瘤中的铂浓度比肝脏高约3.7倍。更重要的是,PMBOP-CP纳米载体不仅对超过5种不同类型的皮下肿瘤模型有靶向作用,在原位肿瘤和肺部转移灶中也有很高的累积。
PMBOP-CP具有肿瘤组织靶向性
与预期一致,PMBOP-CP纳米载体将Xkr8-siRNA递送到肿瘤细胞中,降解了Xkr8的mRNA,降低了Xkr8的蛋白水平,从而明显减少了肿瘤细胞膜外表面磷脂酰丝氨酸的含量。不仅如此,研究人员还发现,在肿瘤细胞与巨噬细胞的共培养实验中,Xkr8-siRNA可以阻断免疫抑制类细胞因子IL-10的分泌,并诱导巨噬细胞向M1群体(免疫激活表型)的分化。
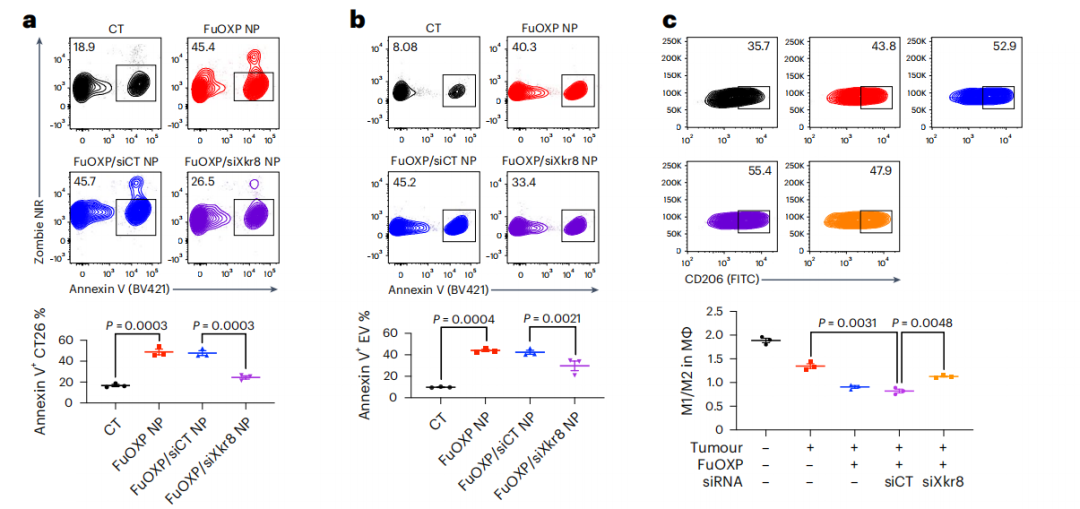
Xkr8-siRNA诱导巨噬细胞的M1极化
最后,研究团队利用PMBOP-CP纳米载体给药结肠癌/胰腺癌小鼠模型,以测试联合用药方案的治疗效果。研究人员发现,相较于单个递送,同时递送铂类药物和Xkr8-siRNA,既能明显减缓小鼠肿瘤的生长速度,又能显着改善肿瘤微环境,大幅增加淋巴细胞、功能性T细胞、M1型巨噬细胞等抗肿瘤免疫细胞的浸润,增强免疫系统对肿瘤细胞的杀伤作用。
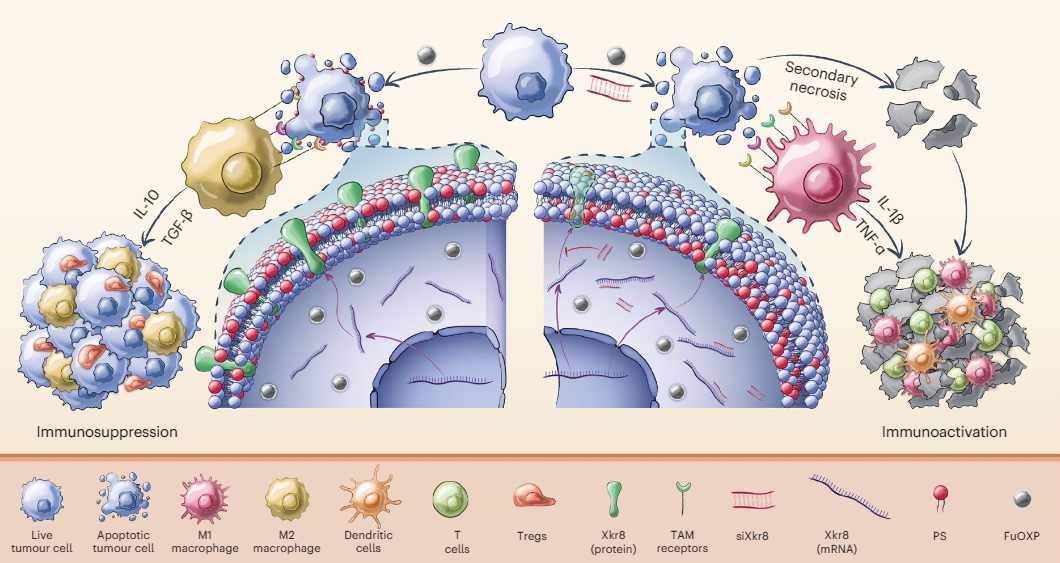
研究模式图
在安全性方面,小鼠对静脉注射PMBOP-CP纳米载体具有良好的耐受性,其在体重、肝肾功能以及几个主要器官的正常组织学等指标均表现正常,证实了PMBOP-CP纳米载体在体内实验中的安全性。
总而言之,这项研究发现铂类药物能显着诱导肿瘤细胞表达促翻转酶Xkr8的表达,进而开发了一种新型纳米载体PMBOP-CP,它可以特异性靶向肿瘤组织,同时递送铂类药物和Xkr8-siRNA,阻断磷脂酰丝氨酸外翻,显着抑制结肠癌和胰腺癌的发展,预示着癌症免疫治疗的新方向。
鉴于他们的目标是将他们的新疗法转化为临床,该团队现在正在寻求通过额外的实验来验证他们的发现,并进一步评估潜在的副作用。
原始出处:
Chen, Y., Huang, Y., Li, Q. et al. Targeting Xkr8 via nanoparticle-mediated in situ co-delivery of siRNA and chemotherapy drugs for cancer immunochemotherapy. Nat. Nanotechnol. (2022). https://doi.org/10.1038/s41565-022-01266-2.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言