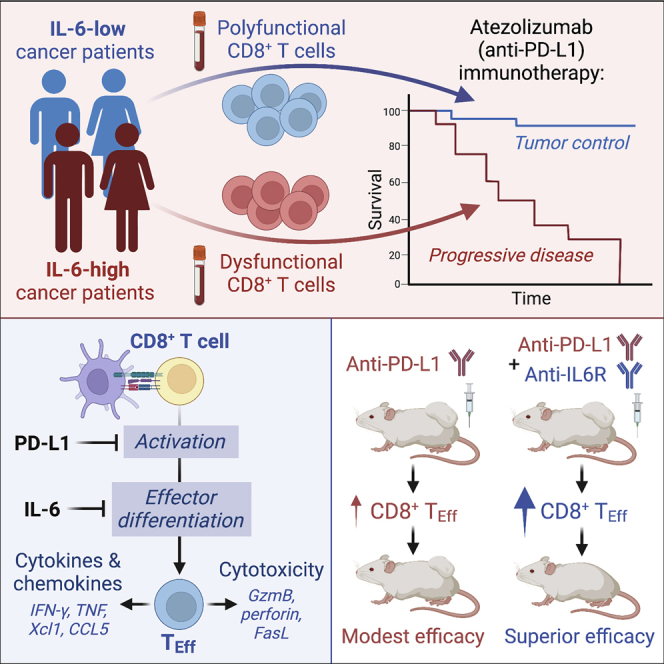
肺癌里,80%是非小细胞肺癌。过去十年里,靶向药和免疫治疗的出现显著延长了肺癌患者的生存时间。其中,非小细胞肺腺癌有大约一半可以使用EGFR靶向药治疗。如果没有靶向药的治疗机会,患者可以选择免疫治疗,这样也可以显著控制疾病和提高患者的生存率。
但是,使用免疫治疗需要检测一些相关指标,其中PD-L1蛋白表达是其中之一,但是基于这个指标预测免疫治疗疗效并非很准确。癌度的上一篇文章就讲过,只有PD-L1的TPS评分大于80%时,单独使用免疫治疗才能获益显著。
基因突变和肿瘤微环境
免疫微环境是指肿瘤周围的免疫细胞和其他细胞的组成和状态。在肿瘤微环境中,免疫细胞可以被肿瘤细胞操纵,从而抑制它们的免疫功能。越来越多的证据表明,肿瘤微环境对患者是否对免疫治疗应答起到重要作用。但是,如何评估肿瘤微环境是一个复杂的问题,因为肿瘤病灶中有多种类型的细胞,包括癌细胞和免疫细胞。
人们发现,EGFR基因突变肺癌的肿瘤微环境里缺乏细胞毒性T细胞;CDKN2A基因突变的肿瘤中,肿瘤免疫炎性途径仅仅是弱表达。因此,基因突变在一定程度上可以预测免疫治疗的疗效。

今天癌度给大家解读的研究报道,是关于肺癌里的另一个基因突变:STK11基因突变。肺癌患者肿瘤里如果存在这种基因突变,会对免疫治疗疗效产生什么样的影响?
STK11基因突变影响免疫治疗
研究者选择研究STK11基因是基于之前的研究成果。共19名尚未接受任何治疗的IA期至IIIB期肺癌患者参加了研究,他们携带KRAS基因突变或者ERBB2(HER2)基因突变。此外,研究者还检测了这些患者肿瘤组织中500个基因的突变情况。
研究结果显示,这些患者的肿瘤病灶具有显著的异质性,而肿瘤病灶内PD-L1的表达异质性较小。换句话说,如果对一个肿瘤病灶的不同部位进行穿刺,检测到的PD-L1表达情况差不多。然而,一个有趣的发现是,STK11基因突变与肿瘤的免疫微环境的“热”或“冷”有关。
冷的免疫微环境是指肿瘤周围免疫细胞数量较少,且这些细胞的活性较低,无法有效地攻击肿瘤细胞。如果STK11基因发生突变,患者的肿瘤病灶更有可能属于冷的免疫微环境,这可能导致免疫治疗效果不佳,并使肿瘤对免疫治疗产生逃逸现象。
至于基因检测套餐里的其他基因,如KRAS、TP53、LRP1B、MTOR、U2AF1等则与肿瘤免疫微环境的“热”或者“冷”无关。
讨论和启示
总体来说,这项发表在《肺癌》期刊上的研究值得我们关注。但是,如果患者没有靶向药治疗的机会,只能选择免疫治疗。这种情况下如果存在STK11基因突变,应该怎么办?难道就不能使用免疫治疗了吗?
这其实这并不是绝对的。我们可以通过适当结合其他治疗方式来改善肿瘤的免疫微环境,例如联合应用抗血管生成靶向药、化疗、放疗等治疗方法,这样有可能改善肿瘤的微环境,增加肿瘤免疫治疗起效的概率。
如果患者没有机会接受靶向药治疗,免疫治疗是至关重要的选择。否则,仅依靠单独的化疗或放疗等传统治疗方法,很难控制癌症,实现长期生存。
.
参考文献:
H. Goldschmid, et al., Spatial profiling of the microenvironment reveals low intratumoral heterogeneity and STK11-associated immune evasion in therapy-naïve lung adenocarcinomas, Lung Cancer (2023)
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言