首例:HER2阳性晚期胃癌获益德曲妥珠单抗三线治疗,取得长期完全缓解
2024-06-18 苏州绘真医学 苏州绘真医学 发表于上海
本文报告了一例维持长期CR的胃癌病例。
德曲妥珠单抗(T-Dxd)已获批用于治疗HER2阳性胃癌。然而,只有部分胃癌患者能够维持长期完全缓解(CR)。本文报告了一例维持长期CR的胃癌病例。一名 60 多岁的女性接受了胃肠镜检查,结果显示前庭小弯处有 2 型病变和溃疡,活检结果显示为腺癌。CT显示胃前区壁增厚,存在转移性肝肿瘤和区域外淋巴结转移;确诊为T4aN3aM1(H,LYN)和cIVB期(HER2 3+)胃癌。最初给予曲妥珠单抗、奥沙利铂和S-1。9 个月后出现腹水,诊断为疾病进展。开始使用紫杉醇和雷莫芦单抗作为二线治疗,但因中性粒细胞减少和腹水增加而停药。开始使用德曲妥珠单抗作为三线治疗,11 个月后CT显示转移消失。在 31 个月后患者仍保持CR。据研究人员所知,这是少数三线使用德曲妥珠单抗治疗并保持长期CR的病例之一。胃癌患者实现长期CR的治疗策略需要仔细考虑。
背 景
抗体药物偶联物(ADC)是一种使用连接子偶联药物载体和细胞毒性药物的生物制药。因此,使用抗体作为载体可以最大限度提高药物靶向治疗的疗效,获得较好的疗效和安全性。人表皮生长因子受体2(HER2)是一种参与癌细胞增殖的蛋白质,在约 20% 的乳腺癌和胃癌中过表达,并且与预后不良和复发有关。德曲妥珠单抗(T-Dxd)是一种单克隆抗HER2抗体和拓扑异构酶I抑制剂偶联的ADC。据报道,T-Dxd不仅对HER2阳性乳腺癌有效,而且对HER2低表达阳性乳腺癌也有效,并广泛用于乳腺癌治疗。
据报道,T-Dxd可用于治疗胃癌。例如,DESTINY-Gastric01试验报告了T-Dxd对HER2阳性胃癌的疗效,T-Dxd于 2020 年在日本获得批准。然而,只有部分病例能够维持长期完全缓解(CR)。本文报告了一例维持长期CR的胃癌病例。
病 例
患者女,60 余岁,因贫血就诊于当地医院。患者有高血压和反流性食管炎病史。患者在上消化道内镜检查时发现胃部肿瘤,随后转诊至日本广岛综合医院。上消化道内镜检查发现胃窦小弯侧有一个 20 mm的 2 型病变,伴有溃疡,活检发现存在高分化腺癌(tub1)(图1a)。CT显示胃窦内有一个肿瘤,胃小弯侧有一个半径为 30 mm的肿大淋巴结,左肾腹侧有肠系膜内淋巴结(图1b、c)。PET-CT扫描显示有明显摄取,肝脏S4段SUVmax为 4.4,小弯淋巴结SUVmax为 7.2(图1d)。根据第八届国际抗癌联盟的诊断为T4aN3aM1(H,LYN)和cIVB期(HER2 免疫组化:3+)胃癌。一线治疗为曲妥珠单抗+S-1+奥沙利铂(曲妥珠单抗,8 mg/kg;奥沙利铂,130 mg/m2;S-1,100 mg)(表1)。患者在第 8 天至第 10 天出现 3 级腹泻和 2 级厌食,使用洛哌丁胺(3.0 mg)和地塞米松(2.0 mg)后有所改善。因腹泻、厌食,分 2 个疗程减量 1 次(曲妥珠单抗 6 mg/kg;奥沙利铂 100 mg/m2;替吉奥 80 mg),3 个疗程后CT复查以进行疗效评价,结果显示胃壁增厚改善,转移性淋巴结缩小(小弯淋巴结 16 mm),判定为部分缓解(图2)。
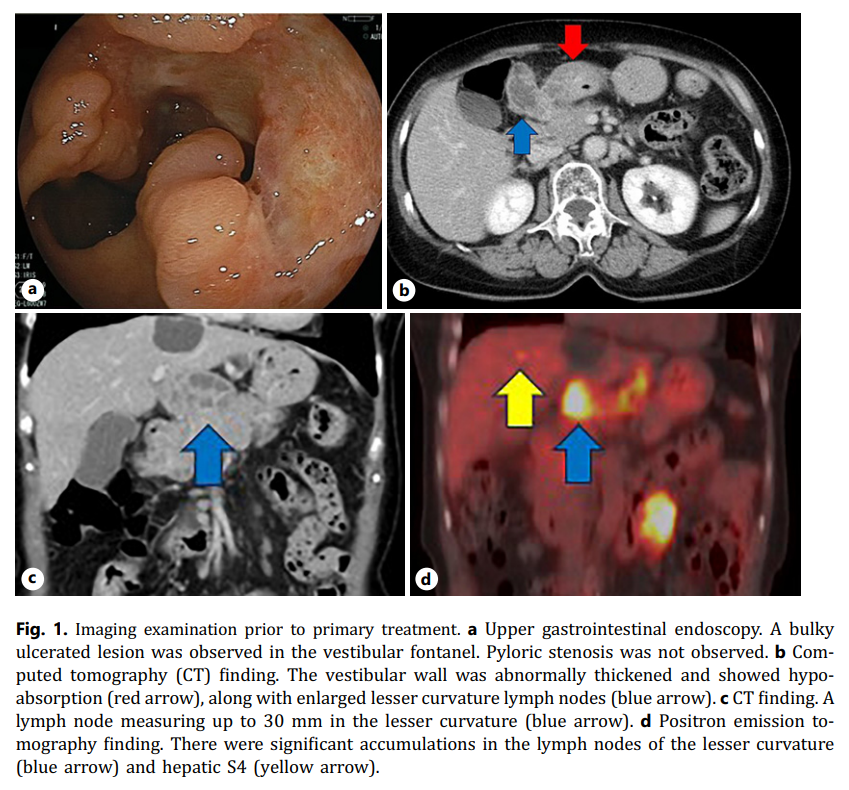
▲图1 初次治疗前的影像学结果
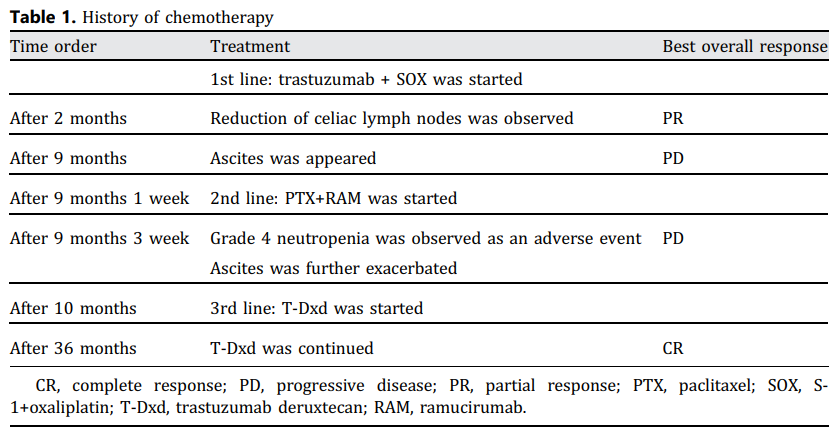
▲表1 化疗史
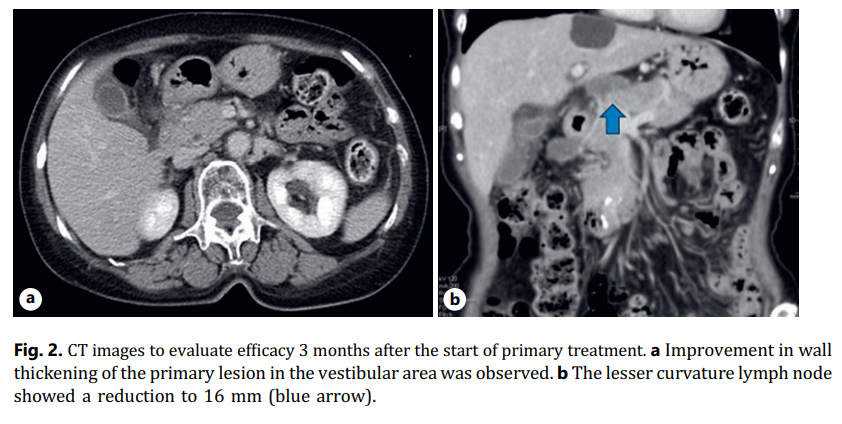
▲图2 治疗三个月后的CT影像,用于疗效评估
在第 12 个疗程时因出现 3 级周围神经病变停用奥沙利铂,随后给予曲妥珠单抗和S-1。然而,治疗开始后 9 个月的CT扫描显示出现腹水和盆腔淋巴结播散,诊断为疾病进展(图3)。二线治疗使用紫杉醇(PTX)(80 mg/m2)和雷莫芦单抗(8 mg/kg)。PTX+雷莫芦单抗治疗 8 天后出现 4 级中性粒细胞减少,通过注射粒细胞集落刺激因子(75 μg)治疗。在进行了一个疗程的二线治疗后,腹水仍持续增加,因此使用浓缩腹水回输术进行治疗;第二个疗程期间给予 80% 剂量的PTX(64 mg/m2);然而,4级中性粒细胞减少再次发生。
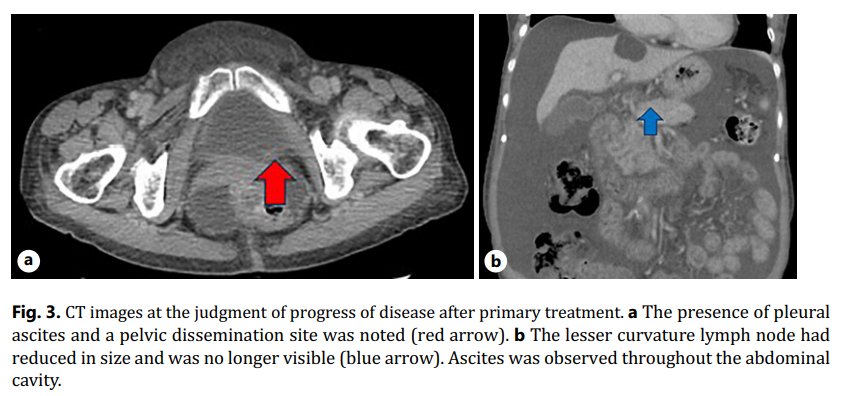
▲图3 初始治疗后判定位疾病进展的CT影像
由于中性粒细胞减少和腹水增加,研究人员确定PTX无法继续应用;因此,开始使用T-Dxd(5.4 mg/kg)作为三线治疗。然而,观察到因肝转移导致的 1 级肝功能障碍。因此研究人员决定对肝功能障碍进行随访。从那时起,肝功能障碍在没有对症治疗的情况下得到改善。2 个月后进行的CT显示胸腔积液减少和部分缓解。11 个月后,上消化道内镜检查显示原发性肿瘤瘢痕形成。30 个月后(43 个疗程),CT显示无明显复发,维持CR(图4a)。又过了 31 个月(共 44 个疗程),上消化道内镜检查显示瘢痕形成,原发病变被正常黏膜覆盖。活检结果显示没有恶性细胞(图4b)。患者目前每 3 周接受一次T-Dxd治疗,观察到 1 级贫血的不良反应。尽管如此,患者仍能正常进行日常活动。
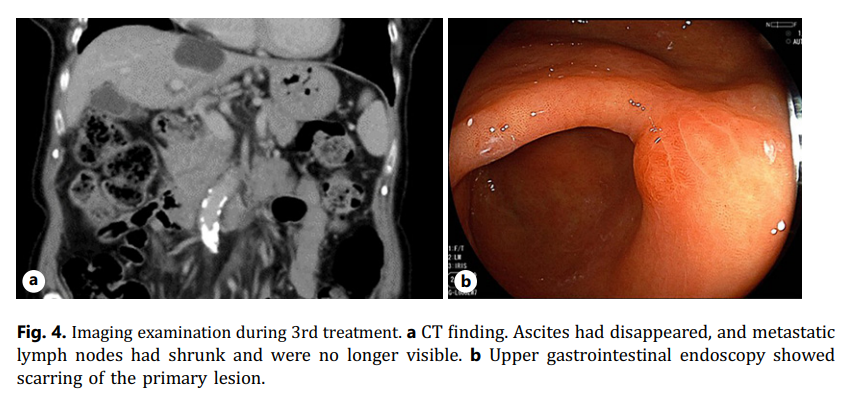
▲图4 三线治疗后的CT影像
讨 论
据研究人员所知,这是首例HER2阳性晚期胃癌患者通过T-Dxd获得长期CR的病例。我们的病例表明,T-Dxd 治疗可长期稳定晚期胃癌。
近年来,已经开发出涉及各种分子(如HER2和PD-1)的胃癌治疗药物和治疗方法。对于未经治疗的胃癌,纳武利尤单抗与标准疗法相结合可改善预后。尽管有几种可靶向HER2阳性胃癌的药物,但帕妥珠单抗和恩美曲妥珠单抗的试验结果为阴性。相反,Tmab(曲妥珠单抗)和T-Dxd显示出积极结果,正在进行开发的药物包括马格妥昔单抗等(margetuximab)。2010 年,ToGA试验证明曲妥珠单抗优于常规化疗,可改善HER2阳性胃癌患者的治疗效果。此外,抗HER2药物被广泛用于治疗胃癌和乳腺癌。T-Dxd是含有DNA拓扑异构酶I抑制剂的第二代ADC。一些研究已经探讨了T-Dxd抗肿瘤作用的潜在机制。有报道称,T-Dxd能被癌细胞内化,进而表现出抗肿瘤活性。此外,由于其具有较好的膜通透性,会渗透到邻近的肿瘤细胞中,预计会产生很高的治疗效果(旁观者杀伤效应)。Nakajima等人报道称,T-Dxd显著诱导HER2阳性胃癌细胞中CXC趋化因子配体(CXCL)9/10/11的mRNA表达。CXCL 9/10/11是T细胞趋化因子,通过其受体CXC趋化因子受体3募集抗肿瘤细胞毒性T淋巴细胞并抑制肿瘤进展。这些结果表明T-Dxd不仅影响肿瘤细胞,还影响周围的免疫细胞,表明其具有抗肿瘤作用。此外,DESTINY-Gastric01试验显示,T-Dxd组的客观缓解率明显高于传统治疗组(42% vs. 12%);CR率也呈现类似趋势(10% vs. 0%)。T-Dxd组的总生存期比传统化疗组长(中位数为 12.5 个月 vs. 8.4 个月)。最近,一项II期试验报告称,T-Dxd对三线治疗后HER2表达较低的胃癌或胃食管交界处癌有效。这些试验表明,HER2表达越高,预后越好。本文患者免疫组化HER2状态为 3+,与先前试验的结果一致。有研究表明,预先给予免疫检查点抑制剂(ICI)和足够的曲妥珠单抗是T-Dxd疗效的有利预后因素。虽然预测T-Dxd给药的治疗反应具有临床价值,但尚未确定。另一方面,有报道称PS(体力状态评分)良好的病例和接受ICI治疗的男性患者的预后更好,这引起了人们对免疫学进一步研究的期待。最近也出现了分子生物学分类,包括Epstein-Barr病毒阳性、微卫星高度不稳定、染色体不稳定和基因组稳定。值得注意的是,DNA损伤反应表达与基因组稳定的胃癌患者的不良预后因素有关。这些生物学分类有可能成为未来化疗和ICI结果的预后因素。在本文案例中,T-Dxd为患者带来了长期CR;但目前尚无明确的预测因素。因此,需要进一步研究以确定T-Dxd给药的预后因素。
化疗、ICIs和分子靶向药物的最新进展大大增强了这些药物的抗肿瘤作用。根据DESTINY-Gastric01试验,T-Dxd三线治显示出达到CR的可能性。因此,患者应继续治疗直至三线治疗。但由于病情进展迅速,胃癌三线治疗的缓解率约为 30%。在本文病例中,二线治疗无法控制癌性腹水;因此,患者在二线治疗早期转入三线T-Dxd治疗,并获得了长期CR。因此,未来可以考虑转化手术(CS)。既往有文献报道曾在使用T-Dxd实现长期CR的病例中实施CS。Yamaguchi等人根据疾病的转移模式将转移性胃癌患者分为四类,并讨论了每类患者的CS和预后(CONVO-GC)。该项研究表明,即使是在具有多种非治愈性因素的患者中,接受R0切除术的患者预后更好。因此,即使对于具有多种非治愈性因素的患者,临床医生也可以在化疗成功且可行手术实现R0切除时考虑CS。在本文病例中,按照CONVO-GC指南,在达到CR后也可考虑CS。然而,本文患者在T-Dxd治疗期间没有同意进行CS,因为不良事件也很少,于是继续进行三线治疗。总之,本文描述了一则使用T-Dxd并实现CR的病例。本文研究结果表明,临床医生必须在适当的时间确定药物序贯治疗策略。
参考文献:
Yamane H, Sugiyama Y, Komo T, Shibata K, Tazaki T, Koyama M, Sasaki M. Long-Term Complete Response to Trastuzumab Deruxtecan in a Case of Unresectable Gastric Cancer. Case Rep Oncol. 2024 Mar 8;17(1):463-470. doi: 10.1159/000537845. PMID: 38464998; PMCID: PMC10923592.

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#胃癌# #三线治疗# #德曲妥珠单抗#
69