PPM:他克莫司剂量/体重调整谷值预测儿童难治性肾病综合征
2022-03-20 从医路漫漫 MedSci原创
肾病综合征(NS)是儿童常见的慢性疾病,临床表现为蛋白尿、低蛋白血症、高脂血症和水肿。他克莫司(TAC,又称FK506)是一种钙调神经磷酸酶抑制剂,是治疗难治性NS患者的一线免疫抑制剂。

背景:肾病综合征(NS)是儿童常见的慢性疾病,临床表现为蛋白尿、低蛋白血症、高脂血症和水肿。他克莫司(TAC,又称FK506)是一种钙调神经磷酸酶抑制剂,是治疗难治性NS患者的一线免疫抑制剂。TAC的药代动力学特点是口服生物利用度低且可变(4~89%),与红细胞结合广泛。TAC是细胞色素P450(CYP)3A和P-糖蛋白(P-gp)的底物,主要以代谢产物(约99%)的形式通过胆道排出。然而,由于治疗窗口狭窄和个体间药代动力学变异大,很难开发出适用于患者的个体化给药方案。治疗药物监测(TDM)需要单独调整TAC剂量。因此,找出影响TAC PK的关键因素,开发预测模型,实现个体化用药具有重要意义。
药物处置和反应的个体差异主要与药物代谢酶、转运蛋白、受体和其他药物靶点的遗传多态性有关。TAC主要由CYP3A代谢,是P-gp1的底物。以往对TAC的研究主要集中在TAC PK通路相关基因(CYP3A、mdr1等)和转录因子编码基因(POR、NR1I2等)的遗传多态性上。CYP3A5*3(Rs776746)是唯一已证实的影响TAC PK的单核苷酸多态(SNPs)。另一方面,由于TAC的高血浆蛋白结合率,肾脏的生理功能也可能导致TAC的个体差异。α-肌动蛋白-4(由ACTN4编码)是肾滤过屏障的关键因子,它的突变可能导致肾脏损害。和之前对Myh9(编码非肌肉肌球蛋白II)的研究表明,Myh9表达的变化可能会损害肾小球滤过屏障。因此,ACTN4和Myh9上的基因多态性也可能影响TAC的浓度。此外,以往关于TAC个体化药物治疗的研究大多是在移植患者中进行的,澄清TAC PK存在较大个体差异的原因。
开发预测模型可以为医生提供可靠、便捷的用药决策支持。然而,只有少数研究建立了儿童难治性NS的TAC群体药代动力学(PPK)模型。Wang等人建立了基于年龄、Cystatin-C和TAC日剂量的TAC PPK模型,而Hao等人发现体重和CyP3A5显著影响TAC PK。然而,Wang等人没有研究遗传多态的影响,Hao等人只研究了CyP3A5的影响,这不能完全解释TAC PK的个体差异。这些限制降低了模型的准确性,限制了它们的临床应用。因此,迫切需要一种简单、准确的基于儿科NS的TAC浓度预测模型,为临床医生制定给药方案提供参考。近年来,基于机器学习的预测模型在疾病的诊断、治疗和预后方面具有良好的性能。Tang等人开发了机器学习模型来预测肾移植患者的TAC稳定剂量,其性能优于传统的统计方法。然而,还没有利用机器学习来预测NS患者TAC浓度的研究。
目的:他克莫司(TAC)是治疗难治性肾病综合征(NS)的一线免疫抑制剂。然而,TAC的药代动力学在患者之间有很高的变异性,因此需要治疗药物监测(TDM)。本研究旨在利用机器学习算法研究临床和遗传变量对难治性NS患儿TAC剂量/体重调整谷浓度(C0/D)的影响,并建立和验证TAC C0/D预测模型。
患者和方法:对171例难治性NS患儿进行TAC治疗后3个月82个临床变量和244个单核苷酸多态(SNPs)与TACC0/D的相关性研究。分别采用极端随机树(ET)、梯度提升决策树(GBDT)、随机森林(RF)、极端梯度提升(XGBoost)和拉索回归等方法建立并验证了预测模型。最好的预测模型在30名难治性NS患者的队列中得到验证。
结果:Gbdt算法在全组(R2=0.444,MSE=591.032,MAE=20.782,MedAE=18.980)和CyP3A5非表达组(R2=0.264,MSE=477.948,MAE=18.119,MedAE=18.771)中表现最好,而ET算法在CYP3A5表达组(R2=0.380,MSE=1839.459,MAE=31.257,MedAE=19.399)中表现最好。这些预测模型包括3个临床变量(ALB0、AGE0和性别)和10个SNP(ACTN4 rs3745859、ACTN4 rs56113315、ACTN4 rs62121818、CTLA4 rs4553808、CYP3A5 rs776746、IL2RA rs12722489、INF2 rs1128880、MAP3K11 rs7946115、Myh9 rs223。
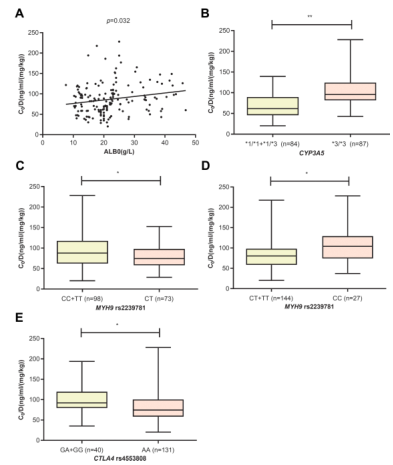
图1 ALB0(A)、CyP3A5(B)、Myh9 rs2239781(C和D)和CTLA4 rs4553808(E)对全组TACC0/D的影响(*p<0.05,**p<0.01)。

图2 CYP3A5等位基因AGE0(A)、MAP3K11 rs7946115(B)、Myh9 rs2239781(C)和CTLA4 rs4553808(D)对TACC0/D的影响(*p<0.05,**p<0.01)。
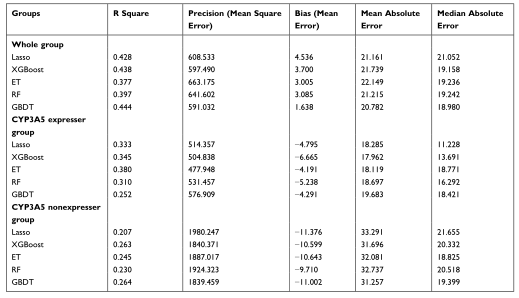
表1全组、CYP3A5表达组和非表达组五种模型在测试集上的性能比较

表2这些预测模型的临床应用情况。将变量输入预测模型后,这些模型最终输出预测的C0/D值
结论:描述了临床和遗传变量与TAC C0/D之间的关系,建立了3种集成临床和遗传变量的TAC C0/D预测模型,并利用机器学习进行了验证,该模型可支持个性化的TAC给药。
原文出处:Mo X, Chen X, Wang X,et al.Prediction of Tacrolimus Dose/Weight-Adjusted Trough Concentration in Pediatric Refractory Nephrotic Syndrome: A Machine Learning Approach.Pharmgenomics Pers Med 2022;15
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#肾病综合征#
94
#他克莫司#
113
#综合征#
0
#难治性#
0